Ионная среда
Cтраница 3
Стеклянный электрод 10 ( типа электрода Бекмана) и мешалка 9 погружены в ионную среду. [31]
Частицы с двойным электрическим слоем ( мицеллы) создают в дисперсной системе соответствующую противоионам ионную среду - суспензионный эффект. Если противоионами являются Н1 - и ОН - ионы, то среда приобретает соответственно кислый или щелочной характер. Суспензионный эффект уменьшается с повышением концентрации электролитов в системе, что связано с сжатием двойного электрического слоя. [32]
Для того чтобы свести к минимуму О-алкилирование дигидро-резорцина, следует проводить процесс в возможно более ионной среде ( гл. [33]
Поэтому лучше прибавлять В и А в виде солей тех форм, из которых состоит ионная среда. [34]
Фоновая соль, конечно, должна быть достаточно растворимой в применяемом растворителе, чтобы дать ионную среду требуемой концентрации. [35]
Тананаева заключается в том, что объем ( плотность) осадка изменяется вследствие изменения коагулирующего воздействия ионной среды с той лишь разницей, что усиление этого воздействия вызывается повышением концентрации ионов-коагуляторов в растворе, а не изменением валентности этих ионов. [36]
Во время измерений коэффициент активности у каждой формы часто можно поддерживать постоянным, например с помощью подходящей ионной среды ( см. гл. [37]
В табл. 8.3 представлены данные, характеризующие зависимость объема осадка Mg ( OH) 2 от воздействия ионной среды. [38]
Конечно, любое сравнение стехиометрических констант должно относиться к значениям, полученным при той же температуре в той же ионной среде. [39]
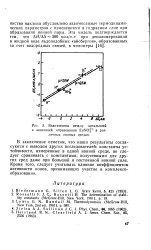 |
Взаимосвязь между энтальпией. [40] |
В заключение отметим, что наши результаты согласуются с выводом других исследователей: константы устойчивости, измеренные в одной ионной среде, не следует сравнивать с константами, полученными для других сред даже при большой и постоянной ионной силе. Кроме того, следует учитывать влияние коэффициентов активности ионов, принимающих участие в комплексо-образовании. [41]
На редокспроцессы влияют: 1) концентрация ионов водорода ( гидроксония ОН1); 2) комплексообразование; 3) ионная среда раствора; 4) образование осадка; 5) экстракция некоторых компонентов реакции. Если в редокспроцессе участвуют ионы водорода, то их концентрация входит в уравнение В. [42]
Константа равновесия (4.21) была измерена [886], и тем самым была определена основность в широком интервале с учетом коэффициентов активности в ионной среде. Данные по алкил-замещенным ароматическим углеводородам [869, 887] ( табл. 4.6) и по незамещенным конденсированным ароматическим углеводородам [886] ( табл. 4.13) были получены именно таким путем. Корреляция этих данных с данными тю измерению электропроводности [783] ( табл. 4.6) не оставляет сомнения в том, что взаимодействие, обеспечивающее экстракцию углеводородов в кислую фазу, приводит к образованию ионов. [43]
В простейшем случае измерения растворимости применяются для изучения равновесия, когда единственными формами, присутствующими в обеих фазах ( кроме растворителя и ионной среды), являются формы, образованные из центральной группы В и лиганда А. [44]
Согласно более простому и широко используемому условию ( Мак-Иннеса) ион хлора, например, имеет один и тот же коэффициент активности в различных ионных средах с одинаковыми ионной силой и моляль-ностьго. [45]
Страницы: 1 2 3 4