Кислая среда
Cтраница 2
Кислая среда указывает на присутствие в пробе свободных кислот, которые даны для анализа или получились в результате гидролиза солей, образованных катионами-слабых оснований и анионами сильных кислот. [16]
Кислая среда, нагревание и в особенности размешивание способствуют собиранию осадка в более крупные творожистые хлопья и осветлению жидкости. [17]
Кислая среда более благоприятствует этому распаду, чем щелочная. [18]
Кислая среда смещает равновесие вправо, щелочная - влево. Однако из-за реакции Н Н Н2 оно быстро нарушается. [19]
Кислая среда более благоприятствует этому распаду, чем щелочная. [20]
Кислая среда указывает на присутствие кислот, фенолов, солей слабых оснований, аминов. Если при смешении раствора органического соединения с раствором соды выделяется COz, то возможно присутствие в молекуле сульфо - или карбоксильной группы. [21]
Кислая среда ( рН 4 5) задерживает развитие бактерий кишечной группы, гнилостных бактерий и палочек ботулизма. [22]
Кислая среда указывает на присутствие в пробе свободных кислот, которые даны для анализа или получились в результате гидролиза солей, образованных катионами слабых оснований и анионами сильных кислот. [23]
Кислая среда благоприятствует образованию а-нзоцианиловой кислоты ( 15 - 20 % при кислотности среды свыше 2W), хотя н метафуль-мннуровая кислота получается в соизмеримом количестве. [24]
Кислая среда способствует процессам, в которых расход ионов Н на восстановление больше расхода ионов ОН - на окисление. В противоположных случаях целесообразно применение щелочной среды. Если же расход Н - и ОН - - ионов одинаков, то реакцию можно проводить и в нейтральной среде. [25]
Кислая среда при этом процессе связана с отнятием иона Н от иона NH -, а не присоединением иона аммония к иону гидроксида. [26]
Кислая среда благоприятствует образованию сьнзоцианиловой кислоты ( 15 - 20 % при кислотности среды свыше 2N), хотя н метафуль-мннуровая кислота получается в соизмеримом количестве. [27]
Кислая среда при этом процессе связана с отнятием иона Н от иона NH -, а не присоединением иона аммония к иону гидроксида. [28]
Кислая среда препятствует росту частиц гидрогеля, что связано с наличием в кислой среде гидратных оболочек вокруг глобул, которые препятствуют срастанию их в частицы большого размера. В присутствии катионов происходит обмен атомов водорода гидро-ксилов. Вероятно, достаточно, чтобы незначительная часть ионов водорода была замещена катионами, тогда в этих местах связь частиц с водой нарушается и соседние частицы будут сцепляться гидрофобными участками. В зависимости от рН среды этот ионный обмен происходит в различной степени и соответственно влияет на пористую структуру ксерогеля. [29]
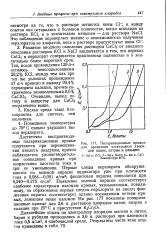 |
Поляризационные кривые для процессов электролиза хлоридов калия, натрия и кальция. [30] |
Страницы: 1 2 3 4