Сильно кислая среда
Cтраница 1
Сильно кислая среда, в условиях которой HNCS менее диссоциирована, препятсгвует реакции; умеренная же кислотность раствора желательна, так как ослабляет гидролиз солей железа. [1]
Сильно кислая среда, в условиях которой HNCS менее диссоциирована, препятствует реакции; умеренная же кислотность раствора желательна, так как ослабляет гидро - лиз солей железа. [2]
В сильно кислой среде ( рН 0 5 и ниже) молибдат свинца растворяется сильнее хромата, вследствие чего тетрагональная система является неустойчивой. [3]
В сильно кислой среде мышьяк ( V) количественно окисляет иодид до иода. [4]
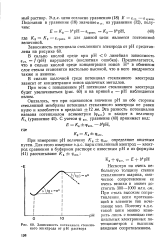 |
Зависимость потенциала стеклянного электрода от рН раствора. [5] |
В сильно кислой среде при рН 0 линейная зависимость ест. Предполагается, что в сильно кислой среде концентрация ионов Н в обменном слое стекла становится настолько высокой, что в него внедряются также и анионы. [6]
В сильно кислой среде при рН менее 2 3, как и в щелочной среде при рН больше 9 7, действие амилазы прекращается. [7]
В сильно кислой среде реакция ( 132) заметно подавляется. [8]
В сильно кислой среде ( рН 2 - 3) образуются преимущественно ППА, вероятно, по последней схеме. [9]
 |
Прибор для определения степени набухания объемным. [10] |
В сильно кислой среде все соли уменьшают набухание; вблизи изоэлектрического состояния соли могут как понижать, так и повышать степень набухания, причем анионы оказывают более сильное влияние, чем катионы. [11]
В сильно кислой среде реакция обратима. [12]
В сильно кислой среде можно обменять эквивалентные количества анионов, но при больших значениях рН наступает изменение степени диссоциации системы из функциональной активной группы и противоиона. Теория мембранного равновесия применима для учета эффекта разбавления. [13]
В сильно кислой среде равновесие смещено в сторону исход-ны продуктов; в нейтральной и, особенно, в щелочной среде за-мещение цианогруппы происходит более легко шо. [14]
В сильно кислой среде происходит, по-видимому, окисление его до соли тетразолия, а в сильно щелочной - вначале, вероятно, отщепление водорода формазанового кольца ( рН 2 13; ЯМакс 520 ммк), а затем разрушение формазана. В кислой среде ( рН 2 5) ФШ также быстро - обесцвечивается, вероятно, вследствие окисления его до соли тетразолия. [15]
Страницы: 1 2 3 4