Сродство - растворитель
Cтраница 1
 |
Значения ГЛБ различных поверхностно-активных веществ. [1] |
Сродство растворителя к поверхностно-активному веществу зависит от размеров и полярности гидрофильных и липофильных групп в молекуле поверхностно-активного вещества. [2]
Диссоциация кислот вызывается сродством растворителя к протону кислоты. Чем больше это сродство, тем легче диссоциирует кислота. Растворители, у которых преобладает сродство к протону, называют протофильными. В протофильном растворителе ( например, жидком аммиаке) очень слабая кислота HCN является сильной. Равновесие реакции HCN NHs - ч - NH - - CN - сдвинуто вправо. [3]
 |
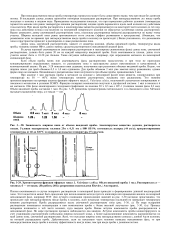
Изотермы адсорбции паров хлороформа ( /, бензола ( 2, диоксана ( 3 и метанола ( 4 на аэросиле. [4] |
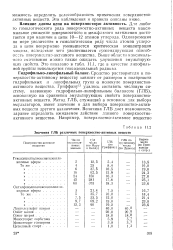
Итак, по величине сродства растворителей к аэросилу можно записать ряд: вода, диметилформамид метанол диоксан бензол хлороформ. Теперь, зная термодинамическое качество растворителей и сродство их к адсорбенту, данные по адсорбции можно объяснить следующим образом. Сополимеры окиси этилена незначительно сорбируются на аэросиле из растворов в ДМФ из-за сильного сродства растворителя к адсорбенту. Величина адсорбции указанных полимеров из растворов в метаноле также невелика по этой же причине, но в данном случае наблюдается резкая зависимость адсорбции от молекулярного веса. Вода является умеренным по силе растворителем для сополимеров окиси этилена и, несомненно, сильно сорбируется на поверхности аэросила; тем не менее адсорбция из воды выше, чем из метанола. [5]
Истинный раствор, благодаря сродству растворителя с растворяемым веществом, образуется самопроизвольно без затраты энергии со стороны, тогда как для образования коллоидного раствора необходима затрата энергии. [6]
Схема показывает, что чем больше сродство растворителей к протону, другими словами, чем больше их основность, тем большее число веществ играет роль кислот. Все вещества, приведенные в схеме, являются кислотами по отношению к аммиаку, только ионы NHg и ОН проявляют в аммиаке свои основные свойства. [7]
НФ и, самое главное, сродства растворителя к неподвижной жидкой фазе. [9]
Большое значение в растворении полимеров имеет растворитель, точнее, сродство растворителя и полимера. Если полярности молекул полимера и молекул растворителя близки, то набухание полимера протекает легко и заканчивается растворением. [10]
Длина зоны, смоченной растворителем, зависит от диаметра колонки, объема введенной пробы, температуры ввода пробы, толщины пленки НФ и, самое главное, сродства растворителя к неподвижной жидкой фазе. [11]
Следует отметить еще одну особенность, отличающую адсорбцию в системе жидкость - твердое тело. Взаимное сродство растворителя и растворенного вещества может сложным образом влиять на количество адсорбируемого вещества. Обозначим Л12 сродство растворителя и растворенного вещества и Ass сродство адсорбента и растворенного вещества. При 4 2 AS2 часть растворенного вещества задерживается в растворе и количество адсорбируемого вещества уменьшается. [12]
Главным достоинством растворителей-экстрагентов являются селективность и эффективность извлечения примесей. Селективность зависит от сродства растворителя к экстрагируемым соединениям и чаще всего определяется относительной полярностью или кислотностью системы растворитель-сорбат. Эффективность десорбции, помимо свойств сорбата и экстрагента, зависит от количественного соотношения растворитель-сорбент. [13]
При самопроизвольном растворении полимера растворитель должен преодолеть его энергию когезии, зависящую от природы полимера и его надмолекулярной структуры. Для растворения необходимо сродство растворителя к полимеру. Качественно это сродство можно оценить эмпирическим правилом: подобное растворяется в подобном. Так, полярные полимеры растворяются в полярных растворителях, неполярные - в неполярных растворителях. [14]
К рассматриваемому вопросу непосредственно примыкает вопрос о характеристике растворяющей способности жидкостей по их физическим свойствам. Однако предварительно следует сделать несколько замечаний о понятии сродства растворителя к полимеру с позиций термодинамики. [15]
Страницы: 1 2