Стабилизация - высшая степень - окисление
Cтраница 1
Стабилизация высших степеней окисления наступает также в случае других галогене комплексов; она становится особенно заметной в присутствии катионов большого объема. [1]
Наконец, стабилизация высших степеней окисления достигается путем комплексообразования с нейтральными лигандами. Энергетически благоприятны здесь прежде всего комплексы с легко поляризующимися лигандами, которые преимущественно связаны ковалентно. [2]
В ряду хлоридов хрома и его аналогов наиболее ярко видна стабилизация высших степеней окисления от хрома к вольфраму. [3]
 |
Некоторые свойства Си, Ag, Аи. [4] |
Для элементов этой подгруппы, как и других побочных подгрупп, наблюдается стабилизация высших степеней окисления с увеличением их: порядкового номера. [5]
 |
Некоторые свойства Си, Ag, Аи. [6] |
Для элементов этой подгруппы, как и других побочных подгрупп, наблюдается стабилизация высших степеней окисления с Евеличением их порядкового номера. [7]
Для элементов подгруппы 1Б, как и других побочных подгрупп, наблюдается стабилизация высших степеней окисления с увеличением их порядкового номера. [8]
Для элементов подгруппы 16, как и других побочных подгрупп, наблюдается стабилизация высших степеней окисления с увеличением их порядкового номера. [9]
 |
Строение молекулы C1F3.| Влияние межъядерного расстояния на степень перекрывания рп - ря-типа. [10] |
Поэтому в роли лигандов эффективнее всего выступают наиболее электроотрицательные атомы ( фтор, кислород), этим же объясняется стабилизация высших степеней окисления элементов в их фторо - и оксо-соединениях. [11]
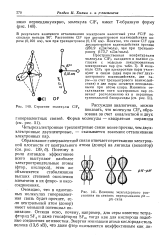 |
Строение молекулы C1F3.| Влияние межъядерного расстояния на степень перекрывания рл - рл-типа. [12] |
Поэтому в роли лигандов эффективнее всего выступают наиболее электроотрицательные атомы ( фтор, кислород), этим же объясняется стабилизация высших степеней окисления элементов в их фторо - и оксо-соединениях. [13]
Отметим, что как для Sn ( - H), так и для РЬ ( 4) известны комплексы типа [ ЭГ6 ] 2 для всех галогенид-ионов, хотя в свободном состоянии РЬВг4 и РЫ4 не существуют. Это обусловлено стабилизацией высшей степени окисления за счет комплек-сообразования. [14]
Отметим, что как для Sn ( 4), так и для РЬ ( 4) известны комплексы типа [ ЭГ6 ] 2 для всех галогенид-ионов, хотя в свободном состоянии РЬВг4 и РЫ4 не существуют. Это обусловлено стабилизацией высшей степени окисления за счет комплек-сообразования. [15]
Страницы: 1 2