Стадия - протонизация
Cтраница 1
Стадия протонизации, которая независимо от каталитического выделения водорода имеет место во многих электродных процессах восстановления органических соединений, была использована для косвенного определения концентрации доноров протона. [1]
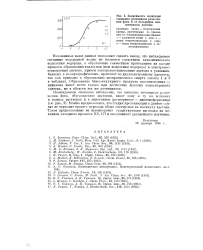 |
Зависимость величины смещения потенциала разложения фона Е от логарифма концентрации ацетона. [2] |
Можно предположить, что стадия протонизации в данном случае не тормозит процесс перехода обоих электронов на молекулу ацетона. Такое предположение не противоречит существующим взглядам на механизм катодного процесса [16, 17] и заслуживает дальнейшего изучения. [3]
 |
Зависимость. 4 / 2 каталитической волны выделения водорода в присутствии пиридина от рН буферного раствора ( ртутный капельный элект. [4] |
Каталитические процессы выделения водорода с объемной стадией протонизации катализатора встречаются сравнительно редко. Гораздо чаще вследствие аначительной адсорби-руемости органических веществ катализатор вступает в реакцию с донором протонов на поверхности электрода в адсорбированном состоянии, что приводит к появлению на поляро-граммах так называемых поверхностных каталитических волн. [5]
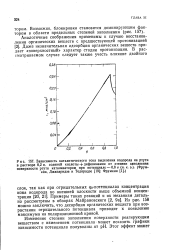 |
Зависимость каталитического тока выделения водорода на ртути. [6] |
Даже незначительная адсорбция органических веществ придает поверхностный характер стадии протонизации. [7]
Напротив, в кислом растворе протекает нуклеофильное замещение через стадию протонизации гидроксильной группы ( образование оксониевой соли) и выделяется бедная энергией вода. [8]
В действительности такие реакции подвержены общему кислотному катализу, хотя из приведенных схем, включающих стадию предварительной равновесной протонизации, следует, что осуществляется специфический кислотный катализ. Общий кислотный катализ может быть в этих случаях логично обоснован, если принять Н3О в качестве одной из возможных кислот, способных к комплексообразованию. [9]
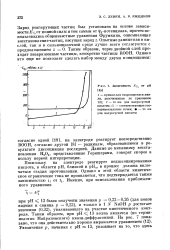 |
Зависимость Еу2 от рН. [10] |
Поскольку на электроде реагирует недиссоциированная кислота, в области рН, близкой к рНа, в процесс должна включаться стадия протонизации. [11]
Ср и Ир могут иметь как диффузионную, так и кинетическую природу. При диффузионном токе стадии протонизации М и U и стадии дегидратации М ( М) - достаточно быстрые, а равновесие стадий об разования аддукта М ( М) не успевает заметно сместиться у поверхности капающего электрода. [12]
Различный характер протекания электровосстановления на платине и ртути был подтвержден сравнением опытных закономерностей с уравнениями (21.9), (21.17) и (21.23), отвечающими трем возможным механизмам электровосстановления. Так, например, электровосстановление нитробензола и ацетона на ртути совершается через стадию поверхностной протонизации. На платине нитробензол восстанавливается при участии адсорбированных атомов водорода, а ацетон вообще не восстанавливается. [13]
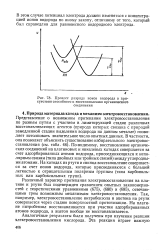 |
Процесс разряда ионов водорода в присутствии способного к восстановлению органического соединения. [14] |
Различный характер протекания электровосстановления на платине и ртути был подтвержден сравнением опытных закономерностей с теоретическими уравнениями ( 675), ( 680) и ( 685), отвечающими трем возможным механизмам электровосстановления. Так, например, электровосстановление нитробензола и ацетона на ртути совершается через стадию поверхностной протонизации. На платине нитробензол восстанавливается при участии адсорбированных атомов водорода, а ацетон вообще не восстанавливается. [15]
Страницы: 1 2