Стадия - дегидратация
Cтраница 3
Такой путь долог, требует присутствия водородных атомов в а-положении к карбонильной функции и может сопровождаться перегруппировками на стадии дегидратации ( стр. [31]
Такой путь долог, требует присутствия водородных атомов в а-положении к карбонильной функции и может сопровождаться перегруппировками на стадии дегидратации ( разд. [32]
Такой путь долог, требует присутствия водородных атомов в а-положении к карбонильной функции и может сопровождаться перегруппировками на стадии дегидратации ( стр. [33]
Свежий двойной суперфосфат предварительно сушат яри температуре около 66 С в течение 1 ч для предотвращения спекания на стадии дегидратации. Просушенный суперфосфат поступает в другую сушилку, где подогревается до 200 - 300 С. [34]
Результаты опытов со смесью меченого бутена, неактивного егор-бутилацетата и уксусной кислоты показывают, что перегруппировка не может включать стадию дегидратации и присоединения уксусной кислоты к олефину, так как сложный эфир не обладает активностью. [35]
Однако, поскольку скорость процесса в этих условиях зависит как от константы равновесия стадии образования продукта присоединения, так и от константы скорости стадии дегидратации, катализируемой кислотами, малая величина р обусловлена взаимным погашением эффектов заместителей на этих двух стадиях. [36]
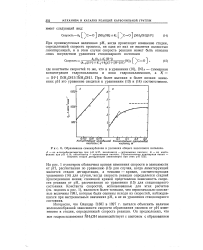 |
Образование семикарбазона в условиях общего кислотного катализа. [37] |
На рис. 1 пунктиром обозначена кривая изменения скорости в зависимости от рН, рассчитанная по уравнению ( 13) для случая, когда лимитирующей является стадия дегидратации, а точками - кривая, соответствующая уравнению ( 14) для случая, когда скорость реакции определяется стадией присоединения амина; сплошной кривой представлена зависимость скорости реакции от рН, рассчитанная по уравнению ( 15) для стационарного состояния. Константы скоростей, использованные для этих расчетов ( см. подпись к рис. 1), являются более точными, чем первоначально описанные величины [98], которые были оценены исходя из скоростей, наблюдавшихся при экстремальных значениях рН, а не из уравнения стационарного состояния. [38]
В целом получение карбамида - гетерогенный процесс в системе Г - Ж, протекающий в кинетической области, причем скорость его лимитируется протекающей наиболее медленно стадией дегидратации карбамата аммония в расплаве. [39]
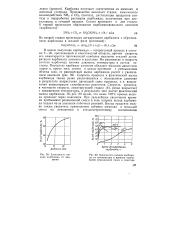 |
Зависимость выхода карбамида от давления.| Зависимость выхода карбамида от температуры и времени пребывания реакционной смеси в реакторе. [40] |
В целом получение карбамида - гетерогенный процесс в системе Г - Ж, протекающий в кинетической области, причем скорость его лимитируется протекающей наиболее медленно стадией дегидратации карбамата аммония в расплаве. На равновесие и скорость синтеза карбамида влияют давление, температура и состав системы. Скорость процесса, в частности скорость лимитирующей стадии ( б), резко возрастает с повышением температуры, в результате чего растет фактический выход карбамида. Из рис. 60 видно, что выше 180 С кривые выхода проходят через максимум. При дальнейшем увеличении времени пребывания реакционной смеси в зоне нагрева выход карбамида падает из-за усиления побочных реакций. [41]
В целом получение карбамида - гетерогенный процесс в системе Г - Ж, протекающий в кинетической области, причем скорость его лимитируется протекающей наиболее медленно стадией дегидратации карбамата аммония в расплаве. На равновесие и скорость синтеза карбамида влияют давление, температура и состав системы. [42]
По другую сторону от нейтральной точки ( в кислой среде) последовательность реакций оказывается катализируемой кислотами; но, как показал Дженкс [156], кислотный катализ проявляется на стадии дегидратации. Это вполне естественно, так как карбиноламин представляет собой псевдооснование и, следовательно, весьма чувствителен к кислотам ( гл. С увеличением концентрации кислоты скорость конденсации может пройти через максимум в некоторой точке, которая соответствует основности присоединившегося амина. При высоких значениях кислотности кислота может так ускорить дегидратацию, что лимитирующей вновь станет стадия присоединения и это приведет к замедлению процесса, так как избыток кислоты выведет первичный амин из реакции, сведя к минимуму его нуклеофильные свойства. [43]
Вслед за Н. Д. Зелинским синтезами простейших индивидуальных углеводородов занимались иностранные химики Кларке [50-53], Эдгар, Калингерт и Маркер [54], Уитмор [55] и др. Применив методику магнийорганиче-ского синтеза, они, переходя стадии дегидратации спиртов и гидрирования непредельных производных, получили шесть из девяти изомеров гептана и все восемнадцать изомеров октана. В 1930 - 1932 гг. Швален, Боурд, Шмидт и другие авторы [56, 57] использовали реакцию между [ 3-бромалкиловыми простыми эфирами и магнием или цинком для получения непредельных углеводородов, из которых затем был приготовлен ряд углеводородов, в частности все тринадцать изомеров гексана. [44]
Относительная легкость присоединения и отщепления углерода в виде карбаниона в основно катализируемых реакциях обусловливает то обстоятельство, что в двухстадийной реакции присоединения карбонильного соединения с образованием ненасыщенного продукта [ схема ( 35) ] стадия дегидратации скорее лимитирует скорость реакции в щелочной, чем в кислой среде. [45]
Страницы: 1 2 3 4