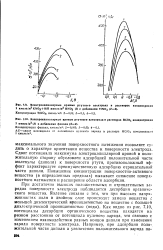
Изменение - заряд - поверхность
Cтраница 2
При пропускании тока в данном случае происходит поляризация идеально поляризуемого электрода, так как все количество введенного электричества идет на изменение заряда поверхности и в общем ( учитывая изменение емкости с изменением потенциала) на увеличение потенциала электрода. [16]
При взаимодействии коллоидов с электролитами, ионы которых могут входить в состав решетки или ионогенных групп частиц, перечисленные эффекты осложняются возможными процессами изменения заряда поверхности, что приводит к еще большему разнообразию электрохимических изменений. [17]
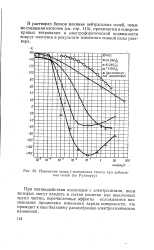 |
Изменение знака - потенциала стекла при добавлении солей ( по Рутжерсу. [18] |
При взаимодействии коллоидов с электролитами, ионы которых могут входить в состав решетки или ионогенных трупп частиц, перечисленные эффекты осложняются возможными процессами изменения заряда поверхности, что приводит к еще большему разнообразию электрохимических изменений. [19]
При е - - v - kT увеличение заполнения происходит в основном за счет увеличения содержания слабой формы хемосорбции и в этом случае практически не сопровождается изменением заряда поверхности. [20]
 |
Влияние комбинированных ингибиторов ( КИ на коррозию цинка в 3 М H2SO4. [21] |
Иными словами, здесь проявляется либо синергизм Топ Тнеорг Торг, либо антагонизм Топ Тнеорр Торг - Можно, однако, сомневаться в том, что в основе синергизма или антагонизма лежит только изменение заряда поверхности и, соответственно, условий адсорбции. Возможно, что присутствие органической добавки изменяет условия контактного выделения металла и структуру образующегося осадка. Синергизму отвечает тот случай, когда осадок становится более гладким и менее пористым, что увеличивает перенапряжение водорода и приближает его к перенапряжению на компактном металле. [22]
Это имеет место, в частности, при образовании заряда на поверхности за счет диссоциации ионогенных групп или тогда, когда переход ионов с поверхности в раствор и наоборот, из раствора на поверхность, требует определенной энергии активации: при наличии барьера изменение заряда поверхности происходит медленнее, чем процесс сближения частиц. В то же время этот барьер не мешает миграции ионов по поверхности, позволяющей принимать, что заряд распределен по поверхности равномерно. [23]
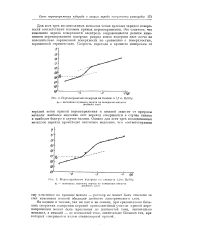 |
Пороиаирижеиие водорода на таллии в 1 7 н. [24] |
Для всех трех исследованных металлов точки нулевых зарядов поверхности соответствуют изломам кривых перенапряжения. Это означает, что изменение заряда поверхности электрода сопровождается резким изменением перенапряжения водорода: разряд ионов водорода идет легче на положительно заряженной поверхности по сравнению с поверхностью, заряженной отрицательно. [25]
Такой вывод следует из принципа тормозящего противодействия Ле-Шателье - Брауна применительно к кинетике химических реакций и из полуэмпирической схемы Эванса - Поляни. Эта схема сильно идеализирована и безоговорочно справедлива лишь в том случае, когда изменение заряда поверхности, обозначаемое через Аф, представляет собой единственный результат воздействия какого-то внешнего фактора, способного влиять на скорость процесса. [26]
На процесс адсорбции ПАВ на поверхности металла в водном растворе электролита могут оказывать влияние механические напряжения. При приложении растягивающих напряжений свободная энергия металла увеличивается, а при неравномерном их распределении может происходить также изменение заряда поверхности. Повышение свободной энергии в общем случае облегчает процесс адсорбции. [27]
В предыдущем сообщении [1] было показано на примере положительных золей окисей металлов, что стабильность может нарушаться или сохраняться без изменений при действии рентгеновского излучения, в зависимости от того, способны ли стабилизирующие комплексы, находящиеся на поверхности частиц, участвовать в окислительно-восстановительных реакциях за счет атомов Н и радикалов ОН, возникающих в воде. Именно протекание таких реакций, возможное, если металлы, входящие в состав комплексов, обладают переменной валентностью, влечет за собой изменение заряда поверхности. В настоящей статье приводятся новые данные, полученные как с положительными, так и с отрицательными золями, подтверждающие правильность представлений, согласно которым изменение стабильности золей при действии излучения определяется только радиационно-химическими реакциями на поверхности частиц и не зависит от знака их заряда. [28]
На рис. 3 приведены характерные электрокапиллярные кривые для чистого раствора сернокислого натрия / и для того же раствора с добавкой соединений, способных адсорбироваться на ртути. Понижение поверхностного натяжения Ау по сравнению с поверхностным натяжением в чистом растворе при данном потенциале указывает на адсорбцию добавленного вещества и на изменение заряда поверхности. [29]
Страницы: 1 2 3