Изменение - заряд - поверхность - металл
Cтраница 1
Изменение заряда поверхности металла происходит не только при его электрохимической поляризации ( например, от внешнего источника), но и вследствие изменения физико-механического состояния поверхности, ведущего к образованию внутреннего двойного слоя при пластической деформации и сдвигу заряда в сторону положительных значений ( гл. [1]
Наблюдаемое при деформации изменение заряда поверхности металла в пределах 0 1 - 0 2 В ( по ср-шкале Л. И. Антропова) в присутствии ингибиторов КПИ-1, АГМИБ и БА-6 еще лежало л в области, где дифференциальная емкость не зависит от потенци-у ала, что обусловлено хемосорбцией этих веществ на железе, как / это было показано экспериментально. [2]
Теория Гельмгольца не объясняет также причины изменения заряда поверхности металла при заданном значении в-потенциала, наблюдаемого в присутствии поверхностно-активных веществ. Вместе с тем теория конденсированного двойного слоя позволяет получить значения емкостей двойного слоя, согласующиеся с опытом, а при использовании экспериментальных величин емкостей - физически правдоподобную толщину двойного электрического слоя. [3]
 |
Зависимость электродного потенциала ( электродной поляризации от плотности тока при выделении водорода на некоторых металлах. [4] |
Эти изменения, как было показано Я. М. Колотырки-ным, связаны с изменением заряда поверхности металла от положительного к отрицательному. Данные табл. 19.1 относятся к отрицательно заряженным поверхностям; они показывают, что диапазон изменения величины а весьма широк: от - 0 1 В для платины, до - 1 5 В для свинца. Помимо материала электрода, на величину а влияет состояние его поверхности. Константа а уменьшается при развитии поверхности и при освобождении ее от поверхностных окислов. Низкие значения b наблюдаются для металлов, обладающих наименьшим перенапряжением ( с минимальной величиной а), например для платины, палладия. [5]
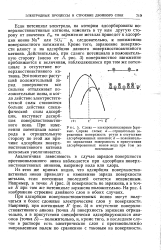
Из этих же кривых видно, что адсорбция поверхностно-активных ионов приводит к изменению заряда поверхности металла, если потенциал последней остается неизменным. Например, в точке А ( рис. 3) поверхность не заряжена, а в точке Б при том же потенциале заряжена положительно. На рис. 4 изображено строение двойного слоя в обоих случаях. [7]
 |
Строение двойного электрического слоя по Гельмгольцу. молекулярная картина ( а и изменение потенциала с расстоянием от поверхности металла в глубь раствора ( б. [8] |
Если заряды, находящиеся в растворе, при относительном движении жидкости и твердого тела связаны только с последним и перемещаются вместе с ним, то - потенциал всегда будет равен нулю. Теория Гельмгольца не объясняет также причины изменения заряда поверхности металла в присутствии поверхностно-активных веществ при заданном значении - потенциала. [9]
 |
Строение двойного электрического слоя по Гельмгольцу. молекулярная картина ( а и изменение потенциала с расстоянием от поверхности металла в глубь раствора ( б. [10] |
Модель двойного электрического слоя, отвечающая этим простейшим представлениям, приводит к двум возможным значениям - потенциала. Если предположить, что все заряды, находящиеся в растворе, способны перемещаться вместе с жидкостью или при движении твердого тела относительно жидкости не увлекаться вместе с ним, то - потенциал по величине - будет совпадать с ( - потенциалом, и его изменение с концентрацией электролита должно подчиняться формуле Нернста. Если заряды, находящиеся в растворе, при относительном движении жидкости и твердого тела связаны только с последним и перемещаются вместе с ним, то - потенциал всегда будет равен нулю. Теория Гельмгольца не объясняет также причины изменения заряда поверхности металла в присутствии поверхностно-активных веществ при заданном значении - потенциала. [11]
Если предположить, что все заряды, находящиеся в растворе, способны перемещаться вместе с жидкостью или при движении твердого тела относительно жидкости не увлекаться вместе с ним, то - потенциал по своей величине будет совпадать с gLM - потенциалом и его изменение с концентрацией электролита должно подчиняться формуле Нернста. Если же заряды, находящиеся в растворе, при относительном движении жидкости и твердого тела связаны только с последним и перемещаются вместе с ним, то - потенциал всегда будет равен нулю. LM) и - потенциалами, ни с опытной зависимостью - потенциала от концентрации, если не считать, что - потенциал может быть равен нулю в очень концентрированных растворах электролитов, или при определенном составе раствора, отвечающем изоэлектрической точке. Теория Гельмгольца не объясняет также причины изменения заряда поверхности металла при заданном значении е-потенциала, наблюдаемого в присутствии поверхностно-активных веществ. Вместе с тем теория конденсированного двойного слоя позволяет получить значения емкостей двойного слоя, согласующиеся с опытом, а при использовании экспериментальных величин емкостей - физически правдоподобную толщину двойного электрического слоя. [12]
Модель двойного электрического слоя, отвечающая этим простейшим представлениям, приводит к двум возможным значениям - потенциала. Если предположить, что все заряды, находящиеся в растворе, способны перемещаться вместе с жидкостью или при движении твердого тела относительно жидкости не увлекаться вместе с ним, то - потенциал по своей величине будет совпадать с gLM - потенциалом и его изменение с концентрацией электролита должно подчиняться формуле Нернста. Если же заряды, находящиеся в растворе, при относительном движении жидкости и твердого тела связаны только с последним и перемещаются вместе с ним, то - потенциал всегда будет равен нулю. Однако равенство - потенциала нулю может реализоваться в очень концентрированных растворах электролитов или при определенном составе раствора, отвечающем изоэлектрической точке. Теория Гельмгольца не объясняет также изменения заряда поверхности металла при заданном значении е-потенциала, которое наблюдается при введении в раствор поверхностно-активных веществ. Вместе с тем теория конденсированного двойного слоя позволяет получить правильные значения емкости двойного слоя, а при использовании опытных величин емкостей - физически правдоподобную толщину двойного электрического слоя. [13]
Страницы: 1