Изменение - значение - потенциал
Cтраница 1
Изменения значений ОВ потенциала, как мы видим, могут быть весьма значительными. [1]
 |
Значения - В / некоторых органических веществ в метаноле и диметилфэрмамиде [ фон EU NJ ]. [2] |
Изменение значений потенциалов полуволн при переходе от одной среды к другой может быть обусловлено рядом различных факторов. [3]
Как видно из табл. 9.12 изменение значений потенциалов происходит колебательно во времени. Примечательным является тот факт, что с повышением температуры от - 11 до 20 С периоды колебаний увеличиваются, а их амплитуды уменьшаются. Такой колебательный процесс, несомненно, обусловливается каталитическим действием гель-иммобилизованной системы, образующейся при насыщении бентонита и других неорганических полимеров ( цеолиты, АСК и др.) метанолом. Действительно, уменьшение амплитуды колебаний связано с устойчивостью молекулярного комплекса метанол - бентонит, образующегося смачиванием метанола. Образование молекулярного комплекса ( А), происходящее за счет сильной водородной связи между метанолом и бентонитом, установлено ИК-исследованиями. Далее молекулярный комплекс ( А) при взаимодействии с ассоциатом воды газового потока переходит в сложный промежуточный комплекс ( Б), который при распаде дает мелкие фрагменты, сопротивляющиеся достижению критического состояния - образованию гидратов. [4]
Пользоваться табл. 16, составленной по изменению значений потенциалов, неудобно, поэтому в приложении 4 дана таблица потенциалов, расположенных в алфавитном порядке по названию металла. [5]
Особая устойчивость этих конфигураций проявляется также в ходе изменения значений потенциалов ионизации в ряду различных ПИ каждого из элементов. В таком ряду ( табл. 18) между двумя определенными соседними значениями ( одно из них подчеркнуто) существует резкий скачок, до и после которого значения ПИ изменяются более или менее плавно. В ряду ПИ атомов Li, Be, В, С, О и F резкий скачок происходит при ПИ, отвечающем отрыву первого электрона из двухэлект-ронного слоя Is2, что подтверждает высокую устойчивость Is2 конфигурации электронов. В ряду атомов Na, Mg, Al и Sc ПИ резко увеличивается при отрыве первого электрона из группировки электронов s 2 6 в соответствии с отмеченной высокой устойчивостью этой группировки. [6]
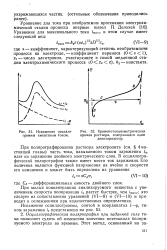 |
Искажение осциллограммы емкостным током.| Хронопотенциометрическая кривая раствора, содержащего один деполяризатор. [7] |
Осциллографическая полярография при заданной силе тока позволяет судить об изменении значения потенциала поляризуемого электрода во времени. [8]
Таким образом, можно полагать, что большие амплитуды колебания потенциалов показывают изменение значений средних мгновенных потенциалов в результате превращения механической энергии в атомную и молекулярную на отдельных группах микронеровностей трущейся поверхности и их разрядов. [9]
Ее можно разложить на составляющие по соответствующим координатным направлениям, каждая из которых равна интенсивности изменения значения потенциала в этих направлениях. [10]
На кинетических кривых ( рис. 4.5 и 4.6) отчетливо видны 2 уча-а: начальный - активного изменения значений потенциала и учас -; стационарного значения, сохраняемого электродом в течение 5 - 10 I. При этом в зависимости от природы соединения для модельных тв лигнина стационарное значение потенциала достигается через JO ч, гидрохинона - через 4 и елового диоксанлигкина - через 36 ч Итакта с окислительно-восстановительной системой. [11]
Указать: а) у элементов каков подгруппы I группы металлические свойства выражены более резко; б) чем объяснить различный ход изменения значений потенциалов ионизации в подгруппах. [12]
Указать: а) у элементов какой подгруппы I группы металлические свойства выражены более резко; б) чем объяснить различный ход изменения значений потенциалов ионизации в подгруппах. [13]
Указать: а) у элементов какой подгруппы I группы металлические свойства выражены более резко; б) чем объяснить различный ход изменения значений потенциалов ионизации в подгруппах. [14]
Из сказанного выше следует, что на основе приведенных в литературе значений констант нестойкости, вычисленных для водных растворов, не содержащих посторонних ионов, можно предусмотреть изменения значений потенциала и полноту связывания данного иона в комплекс только для водных растворов, содержащих потенциалопределяющие ионы и ионы-адденды. Cl -, SO /, то вычисленные константы нестойкости могут не соответствовать фактическим. При введении адденда в соляно - и сернокислые растворы вычисление констант нестойкости нереально. [15]
Страницы: 1 2