Изменение - индикатор
Cтраница 2
Метод контроля за разработкой эксплуатационного объекта ( за направлением и скоростью перемещения нефти, за долей участия в работе пластов многопластового объекта и др.), который основан на наличии определенных закономерностей в изменении естественного индикатора нефти - коэффициента свето-поглощения ( / Ссп - в пределах залежи и на связи динамики изменения этого показателя, определяемого по пробам добываемой из скважин нефти, с перемещением жидкости в пластах. [16]
Когда руководитель замечает опасную тенденцию в изменениях контрольного индикатора, он обязан своевременно принять меры, чтобы затормозить ее и начать подготовку стратегического решения по коренному улучшению складывающейся опасной обстановки. [17]
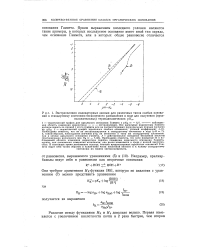 |
Экстраполяция индикаторных данных для различных типов слабых оснований к стандартному состоянию бесконечного разбавления в воде для получения ( предположительных термодинамических рКа. [18] |
Необходимо отметить, что он не экстраполируется к стандартному состоянию в воде ( рН 7), и, таким образом, наблюдаемое значение рНа не относится к тому же стандартному состоянию, как в случае идеального основания Гаммета. Необходимо отметить, что хотя поведение ее в наблюдаемой области изменения индикатора подобно поведению идеального основания Гаммета, однако, как показывают измерения активности, оно резко изменяется в среде с низкой кислотностью. В настоящее время невозможно сказать, сколько предполагаемых идеальных оснований Гаммета ведут себя таким образом в какой-либо части кислотной области и к какому стандартному состоянию их можно экстраполировать. [19]
Даже разрабатывая анкету специально под факторный анализ, включая в нее довольно большое количество наблюдаемых индикаторов, социологи иногда некорректно ставят задачу. Гипотетический латентный фактор ( существование которого априори постулируется) в действительности может не являться причиной, обусловливающей изменения наблюдаемых индикаторов; может быть следствием таких изменений, а может и вообще к таким изменениям не иметь отношения. Фиксация его значений в таких случаях может не приводить к исчезновению связей между наблюдаемыми признаками. Исследователь же, не зная об этом и механически применив технику факторного анализа, либо получает очень плохую модель ( вследствие того что его гипотеза об адекватности факторной модели не отвечает реальности), либо пытается искать интерпретацию найденного более или менее сносного латентного фактора на неправильном пути, полагая, что этот фактор тождествен той самой несостоятельной латентной переменной. [20]
Главное преимущество кондуктометрического метода, по сравнению с применением индикаторов, заключается в возможности экстраполировать эту конечную точку по состоянию раствора до и после эквивалентной ( конечной) точки. Благодаря экстраполяции можно не обращать внимания на состояние равновесий в конечной точке; однако, как раз эти состояния равновесия и делают не резким изменение индикаторов. В индикаторных методах конечная точка определяется из наблюдений в самой конечной точке. Наоборот, при кондуктометрическом методе измерения в этой точке делаются ненужными. [21]
Индикатор, не влияя на ход реакции, дает возможность уловить конец реакции по изменению цвета. Когда реакция между титруемым веществом и титрованным раствором доходит до конца, индикатор в растворе меняет свой цвет или образует муть. Момент, при котором происходят такие изменения индикатора, называется концом титрования. [22]
Точность объемно-аналитических методов часто значительно увеличивается при электрометрическом определении конечных точек, например в случае, когда изменение индикатора обнаруживается недостаточно резко или неточно в надлежащей точке. Именно, отдельные потенциометрические методы вроде титрования галогенидов раствором серебра, были уточнены до такой степени, что точность их достигла точности определений атомного веса. Невидимому, эта возможность имеет значение также и для микроанализа, потому что при титрованиях в очень разбавленных растворах изменения индикаторов часто не резки, или же при вычислениях нуждаются во введении больших поправок на индикатор, чего не требуется при электрометрическом определении. [23]
Эти ошибки связаны только с происходящей химической реакцией и свойствами применяемого индикатора, и они специфичны для каждого данного объемно-аналитического метода. Ошибка титрования будет равна нулю только тогда, когда индикатор изменяется точно в точке эквивалентности. Если он слишком чувствителен, изменение индикатора произойдет раньше этой точки; если чувствительность индикатора мала, мы при титровании перейдем за точку эквивалентности. [24]
Задачи ЕМАР включают описание текущего статуса и определения тенденций экологического состояния оутем измерения индикаторов. Противоречие этих задач в количестве замеров во времени и пространстве; оценка статуса лучше дается при измерении возможно большего количества RSU, в то время как определять тенденции лучше путем повторных измерений одних и тех же элементов выборки. Эти взаимодополняющие подходы разработаны так, что образцы систематической треугольной сетки ( плотность один к четырем) отбираются каждый год, а пробы отдельных RSU отбираются только раз в четыре года. С учетом предварительных работ по моделированию допускается возможность выявления в течение 10 - 15 лет региональных и национальных тенденций изменения индикаторов реагирования при уровне 1 % в год Оценка статуса экологического состояния проводится ежегодно по среднем) - значению за четыре года для четырех различных субсерий. [25]
Титриметрический анализ ( титриметрия) является разделом количественного анализа, в котором количества веществ опреце-ляют путем точного измерения объема ( или массы) раствора реагента ( титранта), вступившего в химическую реакцию с определяемым веществом. Концентрация раствора реагента должна быть точно известна. Раствор реагента с точно известной концентрацией химически активного вещества называется стандартным раствором. Объем раствора реагента, пошедшего на реакцию, точно измеряют, для этого раствор реагента постепенно приливают из бюретки в исследуемый раствор - проводят титрование. Момент, когда реагент добавлен в исследуемый раствор в количестве, химически эквивалентном определяемому веществу ( избыток реагента в отличие от гравиметрии не берется), называется точкой эквивалентности, или теоретической точкой конца титрования. Для определения этого момента в исследуемый раствор добавляют вспомогательное вещество - индикатор. Практически изменение индикатора не точно совпадает с точкой эквивалентности, поэтому говорят о конечной точке титрования. Кроме индикаторных ( визуальных) методов определения точки эквивалентности существует ряд физико-химических, которые в настоящем пособии не рассматриваются. [26]
Для этого колонне придается трубка из стали V2A длиной 20 см и внутренним диаметром 5 мм, наполненная СпО ( величина зерна 0 2 - 0 5 мм), обогреваемая при помощи электрообмотки до 700 С. Получающийся СОг вводится затем в тонкораспыленном виде в камеру титрования. В качестве индикатора служит 0 Q1 % - ный раствор тимолового синего в диметилформамиде. Титруют 0 04 н, раствором щелочи в метаноле. Вода из полиэтиленгликолевых колонн выходит очень медленно, что при применении любых других типов детекторов вызывает длительное колебание нулевой линии. Если применяется наш метод, то поглощенная раствором вода не влияет на изменение индикатора. [27]
Страницы: 1 2