Изменение - концентрация - соляная кислота
Cтраница 1
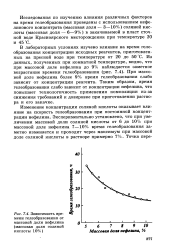 |
Зависимость времени гелеобразования от массовой доли нефелина ( массовая доля соляной кислоты 10 %. [1] |
Изменение концентрации соляной кислоты оказывает влияние на скорость гелеобразования при постоянной концентрации нефелина. [2]
Изменения концентрации соляной кислоты в растворе монохлорида брома, как было установлено, влияют на реакцию двояко. [3]
Изменение концентрации соляной кислоты оказывает влияние на скорость гелеобразования при постоянной концентрации нефелина. [4]
Изменение концентрации соляной кислоты в исследуемом растворе во времени хорошо описывается прямолинейной завн симоет. [5]
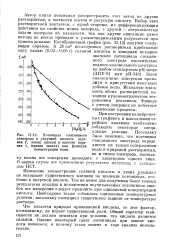 |
Потенциал стеклянного электрода в уксусной кислоте ( кривая 1, левая шкала и ацетоне ( кривая 2, правая шкала как функция концентрации воды. [6] |
Изменение концентрации соляной кислоты в узких пределах не оказывает существенного влияния на значение потенциала, особенно в уксусной кислоте. Тем не менее для получения более точных результатов анализа и исключения неучитываемых источников ошибок все измерения следует проводить при одинаковой концентрации кислоты. Необходимо также соблюдать одинаковые температурные условия, поскольку потенциал существенно зависит от температуры раствора. [7]
При изменении концентрации соляной кислоты от 9 до 13 3 - м, ( рис. 29 и 30) порядок элюирования Am и Cm изменяется точно так же, как при элюировании фтороси-ликатом, причем разделение становится еще более значительным. [8]
Как влияет изменение концентрации соляной кислоты. [9]
Установлено, что в растворе соляной кислоты подвижность ионов Hg2 изменяется с изменением концентрации соляной кислоты. При разделении катионов, об разующих комплексы с ионами Q -, лучшие результаты полу чаются, если подобрать такую концентрацию соляной кислоты, при которой ионы - компоненты смеси образуют комплексы разного заряда. [10]
Установлено, что в растворе соляной кислоты подвижность ионов Hg2 изменяется с изменением концентрации соляной кислоты. При разделении катионов, об-разующих комплексы с ионами С1 -, лучшие результаты полу-чаются, если подобрать такую концентрацию соляной кислоты, ври которой ионы - компоненты смеси образуют комплексы разного заряда. [11]
Полученные данные ( табл. 6) позволяют полагать, что в водных растворах соляной кислоты торий при низких кислотностях сильно гидролизован; он существует в виде ионов ThOH3, ЩОИ) и Th ( OH) 3 и экстрагируется преимущественно как ТЬ ( ОН) С13 X X яДАМФК - Резкое увеличение коэффициента распределения при концентрации соляной кислоты более 5 М объясняется образованием в солянокислых растворах нейтральной соли ТЬС14, экстрагирующейся лучше основных солей. При изменении концентрации соляной кислоты от 1 до 7 М образования заметных количеств анионных комплексов не было обнаружено. [12]
Эти цифры, однако, могут служить только для качественной оценки. Коэффициент распределения изменяется с изменением концентрации соляной кислоты и хлорид-ионов. При экстракции диэтиловым эфиром он проходит через максимум при - 7 М НС1 для Fe ( III), около ЗМ НС1 для Sb ( III), в 4 М НС1 для Sn ( IV); в большинстве других случаев коэффициент распределения повышается с увеличением концентрации кислоты. Последнее связано, возможно, с образованием в эфирной фазе полиядерных комплексов. Механизм процесса, вероятно, заключается в последовательном комплексообразовании в водной фазе с одним или самое большое с двумя комплексами типа МСЬ и НМСЦ, способными к экстракции. При относительно высоких концентрациях галогенидов можно ожидать образования анионных комплексов ( отличающихся от незаряженных форм), что уменьшает экстракцию. [13]
Изучены при помощи радиоактивных изотопов Zn и Gd некоторые свойства трудно растворимых соединений цинка и кадмия, образующихся в системе ион металла - галогенид роданид) - основной краситель. Рассмотрено отношение названных соединений к изменению концентрации соляной кислоты и аниона, а также определена чувствительность отдельных осадителей. [14]
При этом было установлено, что изменение концентрации соляной кислоты оказывает большее влияние на время гелеобразования и пластическую прочность. В то же время, концентрация СРШ сильнее влияет на водородный показатель. [15]
Страницы: 1 2