Изменение - концентрация - раствор - электролит
Cтраница 1
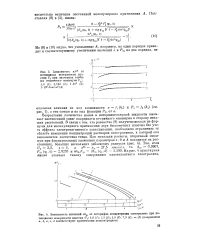
Изменение концентрации растворов электролитов существенно сказывается на коэффициентах активности электролитов. [1]
Для такой ячейки в данных пределах изменения концентрации раствора электролита не наблюдается значительного изменения эквивалентной емкости. [2]
Наиболее полным и точным является анализ зависимости изменения добротности емкостной ячейки от изменения концентрации раствора электролита, находящегося в ней. [3]
На процесс электролитической диссоциации и обратный процесс-ассоциации, ведущий к образованию ( из ионов) молекул, сильно влияет изменение концентрации растворов электролитов. При разбавлении растворов степень электролитической диссоциации электролитов увеличивается. [4]
Если лимитирующими стадиями электродного процесса являются доставка реагентов к поверхности электрода и отвод продуктов реакции путем диффузии, то происходит изменение концентрации раствора электролита или самого электрода у поверхности раздела фаз по сравнению с концентрацией веществ внутри объема фаз. В таком случае поляризация называется концентрационной, а перенапряжение - диффузионным. При замедленности других стадий электродного процесса рассматривают перенапряжение этих стадий. [5]
На процесс электролитической диссоциации и обратный процесс - ассоциации, ведущий к образованию ( из ионов) молекул, сильно влияет изменение концентрации растворов электролитов. При разбавлении растворов степень электролитической диссоциации электролитов увеличивается. [6]
На процесс электролитической диссоциации и обратный процесс - ассоциации, ведущий к образованию ( из ионов) молекул, сильно влияет изменение концентрации растворов электролитов. При разбавлении растворов степень электролитической диссоциации электролитов увеличивается ( см. § 19, стр. [7]
На процесс электролитической диссоциации и обратный процесс - ассоциации, ведущий к образованию ( из ионов) молекул, сильно влияет изменение концентрации растворов электролитов. При разбавлении растворов степень электролитической диссоциации электролитов увеличивается. [8]
Возрастание количества ионов в интермицеллярной жидкости вызывает постепенный сдвиг координаты вторичного минимума в сторону меньших расстояний. В связи с тем, что равенство ( 9) получено исходя из формулы для молекулярного притяжения двух бесконечных пластин без учета эффекта электромагнитного запаздывания, необходимо ограничить ту область изменения концентраций растворов электролитов, в которой оно выполняется достаточно точно. [10]
Непосредственно измеренный сдвиг потенциала при текущей электродной реакции не обязательно равен перенапряжению. Изменение концентрации ионов у поверхности электрода, происходящее вследствие протекающего процесса, сдвигает равновесный потенциал. В таком случае измеренная величина Аф включает в себя две величины: изменение равновесного потенциала вследствие изменения концентрации раствора электролита ( гл. Общее изменение потенциала часто называется поляризацией электрода. [11]
Непосредственно измеренный сдвиг потенциала при текущей электродной реакции не обязательно равен перенапряжению. Изменение концентрации ионов у поверхности электрода, происходящее вследствие протекающего процесса, сдвигает равновесный потен - - циал. В таком случае измеренная величина Аф включает в себя две величины: изменение равновесного потенциала вследствие изменения концентрации раствора электролита ( гл. Общее изменение потенциала часто называется поляризацией электрода. [12]
Непосредственно измеренный сдвиг потенциала при текущей электродной реакции не обязательно равен перенапряжению. Изменение концентрации ионов у поверхности электрода, происходящее вследствие протекающего процесса, сдвигает равновесный потенциал. В таком случае измеренная величина Др включает в себя две величины: изменение равновесного потенциала вследствие изменения концентрации раствора электролита гл. Общее изменение потенциала часто называется поляризацией электрода. [13]
Страницы: 1