Изменение - концентрация - водород
Cтраница 3
Полученные данные показывают, что реакция протекает по первому порядку относительно окиси углерода. Изменение концентрации водорода, углекислоты и водяного пара не влияет на скорость реакции. [31]
 |
Распределение содержания водорода по длине сварного шва, включая кратер ( по данным Н. Кристенсена. [32] |
Кристенсен с сотрудниками провели обширное исследование по распределению водорода в сварном соединении. По характеру изменения концентрации водорода можно сделать вывод, что основная масса водорода успевает выделиться из металла в результате десорбции при образовании шва. [33]
Затем поток газа-носителя проходит через ловушку с адсорбентом, где поглощаются все соединения кроме газа-носителя. Катарометр регистрирует только изменение концентрации водорода в газе-носителе. [34]
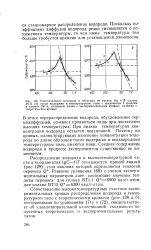
Аналогичными зависимостями на рис. VII.27 показана кинетика изменения концентрации водорода в зоне термического воздействия вблизи границы сплавления для ряда других типовых комбинаций свариваемой стали и металла сварного шва. Так, кривая 2 показывает изменение концентрации водорода во времени для металла из малоуглеродистой стали и шва из высоколегированной хромо-никелевой стали аустенитного класса. В связи с высокой растворимостью водорода в таком металле шва при комнатных температурах водород из шва в зону практически не переходит. Водород из зоны постепенно диффундирует в основной металл и его концентрация в околошовном участке монотонно снижается. [35]
В работе [23] показано, что при окислении водорода на платине наблюдается появление неустойчивого окисла Pt304, который не образуется при прямом взаимодействии платины с кислор одом в отсутствие каталитического процесса. Особенности кинетики этого процесса [24], в частности, наличие экстремумов скорости реакции при изменении концентрации водорода и кислорода, различия наблюдаемых кинетических закономерностей в разных областях концентраций и температур также согласуются с полученными выводами. [36]
I реагируют между собой в соотношении 1: 1, поэтому изменение концентрации йода будет равно изменению концентрации водорода. [37]
Как известно, основным методом регулирования молекулярной массы полимера является введение в реакционный объем водорода. Влияние водорода на скорость полимеризации этилена зависит от состава катализатора, а в случае нанесенных катализаторов - от носителя. Так, изменение концентрации водорода в пределах от 10 до 40 - 50 % ( об.) почти не сказывается на скорости реакции полимеризации этилена при использовании гомогенных ванадиевых катализаторов и катализатора ТМК. Иная картина наблюдается при использовании в качестве носителя хлорида магния: скорость реакции полимеризации этилена резко снижается по Мере увеличения концентрации водорода. [38]
В итоге перераспределение водорода, обусловленное термодиффузией, успевает проявиться лишь при достаточно высоких температурах. При низких температурах концентрация водорода остается неизменной. Поэтому на кривых, иллюстрирующих изменение концентрации водорода по длине образцов после выдержки в неоднородном температурном поле, имеются пики. Среднее содержание водорода в процессе экспериментов существенно не изменяется. [40]
Пополнение катализатора хлором проводится при нормальных температурах риформинга в количестве не более 5 10 % в пересчете на хлор от количества подаваемого сырья. Более интенсивная подача хлора может привести к заметному возрастанию коксообра-зования-на катализаторе. Степень хлорирования ката-лизатора контролируют по изменению концентрации водорода в циркулирующем газе и октановому числу бензина. Перехлорированне катализатора определяют по падению перепада температуры в последней ступени риформинга и резкому увеличению выхода сухого газа прежде всего за счет снижения выхода риформата. [41]
При этом углеводороды проходят через катализатор в потоке газа-носителя, который представляет собой аргон с примесью 5 % водорода. На катализаторе происходят гидрирование олефинов и дегидрирование циклогексанов и нафтенов. Из реактора образовавшиеся углеводороды попадают в ловушку, заполненную активированным древесным углем, адсорбируются и прочно удерживаются в ней. Изменения концентрации водорода в газе-носителе регистрируются катарометром, что помогает идентифицировать эти углеводороды. [42]
 |
Три типа поведения решений системы Лоренца. [43] |
Импульсом для создания математических моделей реальных гетерогенных каталитических систем, в которых возможно возникновение сложных и хаотических колебаний, послужила работа [146], в которой исследован механизм возникновения хаотических колебаний, состоящий из двух медленных и одной быстрой переменной. Большинство математических моделей, описывающих автоколебания скорости реакции на элементе поверхности катализатора, двумерны, поэтому они не пригодны для описания хаотического изменения скорости реакции. Модель учитывает основные стадии процесса: адсорбцию реагирующих веществ, взаимодействие адсорбированных водорода и кислорода, растворение реагирующих веществ в приповерхностном слое катализатора. Показано, что сложные и хаотические колебания возникают в системе с кинетической моделью из трех дифференциальных уравнений, два из которых описывают быстрые процессы - изменение концентраций водорода и кислорода на поверхности катализатора, и третье уравнение описывает медленную стадию - изменение концентрации растворенного кислорода в приповерхностном слое катализатора. [44]
Страницы: 1 2 3