Изменение - равновесная концентрация
Cтраница 1
Изменение равновесной концентрации Mg ( iOH) 2 в водяном паре носит, примерно, такой же характер, как и изменение с температурой плотности пара при постоянном давлении. [1]
Изменение равновесных концентраций реагирующих веществ, вызванное изменением какого-либо условия, называется смещением, или сдвигом, равновесия. [2]
Изменение равновесных концентраций реагирующих веществ, вызванное изменением какого-либо условия, называется смещением или сдвигом равновесия. [3]
Изменения равновесных концентраций реагирующих компонентов, вызываемые присутствием посторонних, но взаимодействующих с ними веществ ( в данном случае маскирующих агентов), учитываются при пользовании реальными константами равновесия. Поэтому реальные константы удобны для выяснения возможностей маскирования. [4]
При изменении равновесной концентрации какого-либо компонента равновесия ( 49) мы вызываем определенное изменение концентрации других компонентов, поскольку Кех постоянна. Разумеется, одновременно можно определить и величину константы экстракции. [5]
 |
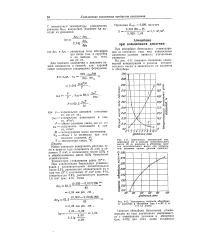
Зависимость равновесного состава газа при 380 С и 300 am. [6] |
Интересно рассмотреть изменение равновесных концентраций компонентов в условиях производства метанола при 50 ат на низкотемпературных медь-цинк-алюминиевых катализаторах. Для расчета принят следующий состав газовой смеси на входе в колонну синтеза: 16 объемн. При расчете учитывалось, что одновременно с реакцией образования метанола идет реакция восстановления СО2 водородом. [7]
Процесс титрования сопровождается изменением равновесных концентраций реагента, определяемого в-ва и продуктов р-ции. [8]
На рис. 1.2 а показано изменение равновесных концентраций СО2, СО, Н2О, Н2 в интервале избытков воздуха от 0 6 до 1 1 при отвечающей ядру горения факела температуре 1600 С. Как видно из графика, для обоих топлив наблюдается рост парциальных давлений СО и Н2 по мере уменьшения избытка воздуха. Парциальные давления СО2 и Н2О лри этом уменьшаются. [9]
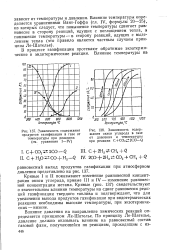 |
Зависимость содержания.| Зависимость содержания окиси углерода в газе от давления и температуры при реакции С СО2 2СО - Q. [10] |
Кривые I и II показывают изменение равновесной концентрации окиси углерода, кривые III и IV - изменение равновесной концентрации метана. Кривые ( рис. 137) свидетельствуют о значительном влиянии температуры на сдвиг равновесия реакций газификации твердого топлива и подтверждают, что для увеличения выхода продуктов газификации при эндотермических реакциях необходимы высокие температуры, при экзотермических - низкие. [11]
Это означает, что область изменения равновесной концентрации данного мономера ограничена площадью, указанной на рис. II.4. Такое утверждение справедливо в том случае, если константа равновесия при сополимериза-ции определяется только последним эвеном в полимерной цепи. [12]
Это означает, что область изменения равновесной концентрации данного мономера ограничена площадью, указанной на рисунке. Это утверждение справедливо в том случае, если константа равновесия при сополи-меризации определяется только последним звеном в полимерной цепи. [13]
Позволяет ли принцип Ле Шателье предсказать изменение равновесных концентраций для следующих реакций, если смесь газов сжимается. Если это так, то в какую сторону смещается равновесие - в сторону образования реагирующих веществ или продуктов реакции. [14]
Страницы: 1 2 3 4