Диселениды
Cтраница 2
Диселенид никеля NiSe2 в виде хрупкой массы серо-черного цвета получается при взаимодействии хлорида или окиси никеля с селеноводородом при температуре 300 С. Селениды никеля при нагревании в токе водорода до температуры 800 С постепенно теряют селен. В результате получается расплавленная масса желто-бронзового цвета. [16]
Диселенид палладия PdSe2 был получен [416] нагреванием двуххлористого палладия с избытком селена в инертной атмосфере ( углекислый газ, азот) при температуре несколько более 600 С. [17]
Диселенид платины PtSe2 был получен Томасеном [415] синтезом из простых веществ. [18]
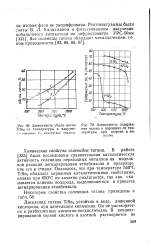 |
Зависимость убыли массы [ IMAGE ] Зависимость содержа - TiSe2 от температуры в вакууме. ния селена в порошках от тем - / - порошки. 2 -компактные образцы пературы при нагреве в вакууме. [19] |
Диселенид титана TiSea устойчив в воде, лишенной кислорода, при длительном кипячении. Он не растворяется в разбавленных кислотах-неокислителях. [20]
Диселенид кобальта CoSeg получается при взаимодействии хлорида кобальта с селеноводородом при температуре 60 - 700 С. [21]
Те диселениды, которые содержат два атома селена рядом, пахнут так же отвратительно, как селеновые меркаптаны. [22]
Аналогичный диселенид получают действием СН С12 на расплавленный селен; он имеет более неприятный запах, чем CS. [23]
Аналогичный диселенид получают действием СН2С1, на расплавленный селен; он имеет более неприятный запах, чемСЗ, нов отличие от него не воспламеняется. [24]
Стеклообразный диселенид кремния ввиду меньшей реакционной поверхности более химически стоек, чем кристаллический - Однако вода разлагает его при комнатной температуре, а концентрированная серная кислота растворяет с зеленым окрашиванием при продолжительном нагревании. Водный раствор NaOH быстро разлагает стеклообразный диселенид кремния с образованием красного раствора полиселенида натрия. [25]
Почти все диселениды тяжелых металлов, за исключением теллуридов, имеют более низкие коэффициенты трения. Очень низкие коэффициенты трения WSe2, NbSe2, TaSe2 обусловлены большими размерами атомов металла, в результате чего ослабляются силы Ван-дер - Вааль-са и более легко расщепляется простая структура. [26]
На воздухе диселенид вполне устойчив. В концентрированной соляной кислоте даже при нагревании устойчив; в азотной, серной кислотах и царской водке несколько растворяется. [27]
Так как диселенид урана встречается в виде трех полиморфных модифн - аций, для получения какой-либо из них необходимо создание определенных условий синтеза. Приведенные ниже методики позволяют направленно синтезировать различные модификации. [28]
Аналогично дисульфидам восстанавливаются диселениды. [29]
Аналогично дисульфидам восстанавливаются диселениды. [30]
Страницы: 1 2 3 4