Степень - дисперсность - коллоидная система
Cтраница 1
Степень дисперсности коллоидных систем характеризуется обычно линейными размерами частиц: чем больше размер частиц, тем меньше степень дисперсности и наоборот. [1]
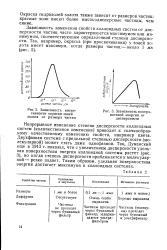 |
Зависимость поверхностной энергии от дисперсности. [2] |
Непрерывное изменение степени дисперсности коллоидных систем ( количественное изменение) приводит к скачкообразному качественному изменению свойств, например цвета. Двухфазная система с предельной степенью дисперсности ( молекулярной) может стать даже однофазной. Так, Думанский еще в 1913 г. показал, что с увеличением дисперсности удельная поверхностная энергия коллоидной системы растет ( рис. 3), но когда степень дисперсности приближается к молекулярной-резко падает. Таким образом, удельная поверхностная энергия достигает максимума в коллоидных системах. [3]
Непрерывное изменение степени дисперсности коллоидных систем ( количественное изменение) приводит к скачкообразному качественному изменению свойств, например цвета. Двухфазная система с предельной степенью дисперсности ( молекулярной) может стать даже однофазной. Так, Думанский еще в 1913 г. показал, что с увеличением дисперсности удельная поверхностная энергия коллоидной системы растет ( рис. 3), но когда степень дисперсности приближается к молекулярной - резко падает. Таким образом, удельная поверхностная энергия достигает максимума в коллоидных системах. [4]
Очевидно, что степень дисперсности коллоидной системы, ее агрегатное состояние и скорость разрушения с выпадением твердой фазы в значительной мере зависят от химического состава нефтепродуктов. [5]
Степень дисперсности в коллоидных системах имеет такое же значение, как молекулярный вес в химии: так же, как и молекулярный вес, несмотря на его важность в химии, не может определять все свойства вещества, степень дисперсности коллоидных систем не определяет всех их свойств. [6]
Водно-коллоидные растворы хлорофилла получаются при смешении молекулярного раствора этого пигмента ( в спирте или ацетоне) с водой. Спектр такого коллоидного раствора зависит от условий смешивания; по этой причине наблюдались расхождения в положениях максимумов полос коллоидного хлорофилла, полученных прежними исследователями. Губерт нашел, однако, что положение максимума зависит от степени дисперсности коллоидной системы; добавление хлористого магния, который обусловливает рост частиц и в конце концов приводит к флоккуля-ции, сдвигает максимум на 8 му. [7]
 |
Коллоидные частицы свежеприготовленного золя сернистого мышьяка.| Иглообразные формы. [8] |
Ею было установлено, что сначала образуются шарообразные или бесформенные частицы, имеющие аморфную структуру. В дальнейшем же внутри аморфных частиц возникают кристаллы. Процесс кристаллизации протекает во времени. Степень дисперсности коллоидных систем зависит от концентрации присутствующих электролитов при образовании коллоидной системы. [9]
 |
Схема воронки с ультрафильтром. / - мембрана. 2 - пористая пластинка. 3 - воронка.| Относительные скорости очистки коллоидных растворов. [10] |
Тиндаль заметил, что если пропустить пучок сходящихся лучей через коллоидный раствор, то наблюдается образование светящегося конуса. Это явление в честь автора названо явлением Тиндаля. Первоначально - предполагали, что этим свойством обладают только коллоидные системы. Но впоследствии было найдено, что явление Тиндаля наблюдается у всех дисперсных систем, степень дисперсности которых равна или больше степени дисперсности коллоидной системы. [11]
 |
Схема строения коллоидной частицы иодида серебра. [12] |
Например, в случае асимметрического строения частиц коллоидные системы проявляют свойство к образованию внутренней сетчатой структуры. Было установлено, что сначала образуются шарообразные или бесформенные частицы, имеющие аморфную структуру. В дальнейшем же внутри аморфных частиц возникают кристаллы. Процесс кристаллизации протекает во времени. Степень дисперсности коллоидных систем зависит от концентрации присутствующих электролитов при образовании коллоидной системы. [13]
 |
Схема, демонстрирующая уменьшение общей поверхности раздела при агрегации коллоидов. [14] |
При определенных условиях происходит уменьшение поверхностной энергии за счет уменьшения поверхности гетерогенной дисперсной системы. Kat известно, коллоидные частицы харак теризуются интенсивным броуновскиь движением. Ясно, что при этом вероятност) столкновений между отдельными части цами весьма велика. На поверхносп каждой частицы имеются неиспользо ванные силы сцепления. При столкнове нии коллоидных частиц друг с другоь происходит их связывание; неиспользо ванные силы сцепления в местах столк новения взаимно насыщаются. Из не скольких свободно двигающихся части. Таким образом, происходит агрегация коллоидных частиц, в результате которой степень дисперсности коллоидных систем уменьшается. Уменьшение степени дисперсности влечет за собой уменьшение общей поверхности раздела и следовательно, уменьшение поверхностной энергии. Последняя используется на производство агрегации. Приводимая на рис. 77 схема показывает это уменьшение поверхности при агрегации. [15]
Страницы: 1