Степень - диссоциация - комплексный ион
Cтраница 1
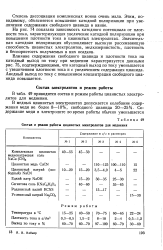 |
Состав и режим работы цианистых электролитов для меднения. [1] |
Степень диссоциации комплексных ионов очень мала. Этим, по-видимому, объясняется повышение катодной поляризации при увеличении содержания свободного цианида в ванне. [2]
Избыток лиганда влияет на степень диссоциации комплексного иона, уменьшая ее, что приводит к более полному связыванию мешающего иона. [3]
Добавление спирта п соляной кислоты в смесь уменьшает степень диссоциаций комплексного иона, окраска исчезает. [4]
Между комплексными и двойными солями существуют переходы, в зависимости от степени диссоциации комплексного иона на отдельные ионы. Поэтому говорят о степени комплексообразовательной способности и делают различие между малодиссоциированными, сильно комплексными и сильно диссоциированными, слабо комплексными ионами. Примером различной степени комплексообразовательной способности могут служить вышеупомянутые комплексные аммиачные соединения серебра. [5]
Наличие в растворе посторонних ионов в ряде случаев также оказывает влияние на чувствительность реакции вследствие изменения растворимости вещества или степени диссоциации комплексного иона. Кроме того, определяемый ион может давать с посторонним ионом комплексное соединение. [6]
Многие хорошо растворимые комплексные соединения можно разрушить действием других электролитов или растворителя, если в результате образуются малорастворимые соединения или новые комплексные ионы, степень диссоциации которых меньше степени диссоциации исходного комплексного иона. [7]
Сдвиг равновесного потенциала зависит от природы металла и комплексообразователя. Величина сдвига потенциала определяется степенью диссоциации комплексного иона. [8]
Приведенные на этом рисунке данные также показывают, что с понижением общей концентрации электролита стационарный потенциал палладия смещается в положительную сторону. Такое явление обусловлено, как и в других комплексных электролитах, увеличением степени диссоциации комплексных ионов при разбавлении раствора. [9]
Значительно более эффективным методом сближения потенциалов соосаждаемых металлов является комплексообразование. Сдвиг равновесного потенциала при комплексообразовании зависит от природы металла и лиганда. Величина сдвига потенциала определяется степенью диссоциации комплексного иона. Так, осаждение сплава Си-Zn становится возможным при использовании цианидных растворов. [10]
Страницы: 1