Степень - диссоциация - ионогенная группа
Cтраница 2
С-отрицательный логарифм кажущейся константы диссоциации ионита; п - постоянная, характеризующая степень структурирования полимера; а - степень диссоциации ионогенных групп. [16]
Эта аномалия обусловлена диффузией компенсирующих ионов из окружающего макромолекулы ионного облака в чистую воду и связанным с этим увеличением степени диссоциации ионогенных групп и размера макромолекул. В присутствии сильных электролитов, подавляющих диссоциацию ионогенных групп, аномалии приведенной вязкости не наблюдается. [17]
Подробный анализ свойств ионообменных смол, отличающихся по химической структуре элементарных ячеек макромолекул, позволяет наметить одновременно и иной путь изменения степени диссоциации ионогенных групп смолы. Известно большое число разнообразных слабокислотных катионообменных смол, содержащих карбоксильные и оксифениль-ные группы, обладающие различной степенью диссоциации, несмотря на то, что указанные сорбенты содержат одинаковые кислотные группы. [18]
Важной характеристикой ионитов является их поглощающая способность, или обменная емкость, зависящая от ряда факторов, и прежде всего от числа ионогенных групп в единице объема. Степень диссоциации ионогенных групп, зависящая от природы ионита и свойств раствора, определяет кислотные и основные свойства ионита. [19]
Повышение температуры в раствбрах высокополи-меров увеличивает осмотическое давление в большей степени, чем это следует из вышеприведенной формулы. Это обусловлено повышением степени диссоциации ионогенных групп белков и их дезагрегацией на микроглобулы. Дополнительная гидратация последних уменьшает количество свободного растворителя, что равносильно увеличению концентрации частиц в растворе. [20]
Повышение температуры в растворах высокополимеров увеличивает осмотическое давление в большей мере, чем следует из теоретического расчета. Это зависит от повышения степени диссоциации ионогенных групп белков и от дезагрегации белков на микроглобулы. Дополнительная гидратация микроглобул уменьшает количество свободного растворителя, что соответствует увеличению концентрации частиц в растворе. [21]
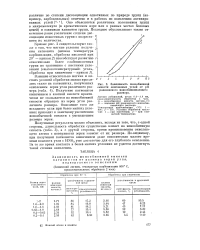 |
Зависимость ионообменной. [22] |
Оно объясняется различным положением групп в макромолекуле ( в ароматическом ядре или в разных местах боковых цепей) и взаимным влиянием групп. Последнее обусловливает также отмеченное ранее увеличение степени диссоциации ионогенных групп с возрастанием их количества. [23]
 |
Влияние степени спшкки на обменную емкость сильноос нонных анионитоп типов I и II и С1 - форме.| Краткая характеристика отечественных. [24] |
Она, как и другие физико-химич. Ембу-хание, прочность и др.), зависит не только от концентрации и степени диссоциации ионогенных групп в фазе смолы, но и от структуры ионообменного материала, определяющей степень доступности функциональных групп для обменивающихся ионов и кинетику ионного обмена. [25]
 |
Элементарный состав ( в вес. % некоторых ионитов в Н - форме. [26] |
Таким образом, наблюдавшиеся закономерности полностью подтверждают важную роль селективной проницаемости гранул ионитов. Проникновение внутрь гранулы противоионов облегчается, а вторжение коионов затрудняется тем сильнее, чем выше степень диссоциации ионогенных групп и их объемная концентрация в ионите. Это обстоятельство необходимо всегда учитывать в процессах изготовления ЭЙ. [27]
В результате изучения влияния низкомолекулярного электролита ( хлорида натрия), содержащегося в сточной воде, на зависимость - потенциала от дозы флокулянта, установлено, что с увеличением содержания хлорида натрия до 1 5 г / л наблюдается более резкое уменьшение отрицательной величины - потенциала при добавлении флокулянта. Дальнейший рост содержания хлорида натрия в сточной воде сопровождается замедлением снижения g - потенциала, увеличением оптимальной дозы флокулянта и ухудшением эффекта очистки. Это обусловлено снижением степени диссоциации ионогенных групп флокулянта, свертыванием макромолекул и уменьшением их суммарного положительного заряда. [28]
Существуют как твердые макроионы ( глобулярные белки и др.), так и гибкие полиэлектролитные цепи. Очевидно, что свойства таких макромолекул существенно зависят от взаимодействия содержащихся в них зарядов. Величины этих зарядов определяются степенями диссоциации ионогенных групп и окружающей их ионной атмосферой. [29]
Наличие сильно разветвленных вторичных структур для полиакрилатов натрия, цезия и четвертичных аммониевых оснований следует ожидать, если при рассмотрении конфигурационного состояния гибких полиионов в растворе исходить из соотношения между термическими силами, стремящимися свернуть цепочку в клубок, и электростатическими силами между заряженными звеньями цепи, приводящими к увеличению ее жесткости. И действительно, когда мы имеем дело со слабым полимерным электролитом ( как было показано выше для случая полиакриловой кислоты в водном растворе), молекулы которого ионизированы только частично, полиион будет обладать формой компактного и более или менее диффузного клубка, так как внутримолекулярные электростатические силы отталкивания невелики и недостаточны для выпрямления молекулы, способствуя только расширению клубка. При введении в цепочку слабого полиэлектролита катионов, способствующих увеличению степени диссоциации ионогенных групп, а следовательно и возрастанию эффективного заряда цепи, следует ожидать возрастания внутримолекулярных электростатических сил отталкивания, а следовательно и жесткости цепи. Когда эти силы начинают превосходить термические, молекулярная цепочка начинает выпрямляться, приобретая форму вытянутой жесткой палочки. Следовательно, в растворах полиакрилатов натрия, цезия и четвертичных аммониевых оснований молекулярные цепочки будут предельно распрямлены. И далее, предельно асимметричные молекулярные цепочки агрегируют параллельным соединением друг с другом с образованием фибрилл, переплетение которых и дает нам сетки - вторичные структуры. Отдельные фибриллы имеют величины поперечных размеров, колеблющиеся в пределах 40 - 120 А. Исходя из значения расстояний между компактно уложенными молекулярными цепочками ( 3 А) и величин поперечных размеров самой молекулярной цепочки ( 4 5 А), для случая предельной асимметрии, когда молекулы имеют форму вытянутой палочки, мы можем считать, что фибриллы составлены из 5 - 16 молекулярных цепочек, соединенных друг с другом в пачки. Следует отметить то обстоятельство, что и в сильно разбавленных растворах, где не имеет места образование вторичных структур из-за малой концентрации вещества, не происходит распад пачек; они продолжают существовать, приобретая из-за присущей им гибкости сильно изогнутую форму. [30]
Страницы: 1 2 3