Степень - набухание - ионит
Cтраница 3
Однако в отдельных, сравнительно редких случаях величина АФнаб Для системы органический ион-ион металла ( или другой малый симметричный ион) уменьшается с ростом степени набухания ионитов, что вызывает увеличение избирательности сорбции более селективных ионов. Обе возможности представлены в табл. 3.3, где ДФнаб относится к состоянию ионита, приближающемуся к максимальному заполнению ионита органическими противоионами. [31]
В средах с низкой диэлектрической проницаемостью скорость процесса на обычных гелевых ионитах в десятки раз меньше, чем в водных средах, что объясняется малой степенью набухания ионитов. Попытки применить в таких средах олеофильные иониты, способные к большему набуханию, оказались мало успешными. [32]
 |
Характер изменения концентрации ионов А и В на различном расстоянии от центра частицы ионита при гелевой кинетике ионного обмена. [33] |
В реальных условиях на кинетику ионного обмена, помимо рассмотренных выше факторов и параметров, определяющих скорость взаимодиффузии ионов, влияет ряд дополнительных, в первую очередь таких, как возникновение электрического потенциала, изменение степени набухания ионита и коэффициентов активности и некоторые другие. [34]
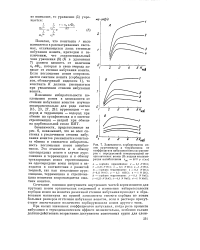
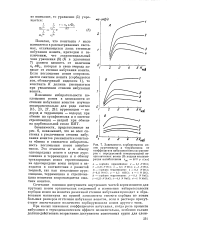
Сочетание влияния доступности внутренних частей зерен ионитов для крупных ионов органических соединений и изменения избирательности сорбции ионов на ионитах различной степени набухания приводит к образованию максимума на кривой зависимости емкости сорбции по ионам больших размеров от степени набухания ионитов, если в растворе присутствует значительное количество сорбирующихся ионов другого типа. [36]
ДВБ) и их влияние на прецессионного обмена могут быть охарактеризованы следующим образом: во-первых, концентрацией диви-нилбензола определяются кинетические свойства ионитов, играющие большую роль в процессе ионного обмена; во-вторых, числом поперечных связей и их химическими свойствами определяются степень набухания ионита, от которой зависит изменение жнной силы в смоляной фазе, степень гидратации ионогенных групп и сорбированных ионов, и, наконец, по мере увеличения числа поперечных связей увеличивается химическая стойкость ионита. Наряду с влиянием числа поперечных связей на процесс ионного обмена немалое влияние оказывают число и расположение ионогенных групп в ионите. Для выяснения этого вопроса был изучен обмен разно - и равнозарядных анионов в системах RH-NaCl, RH - СаС12 и RNa-CaCU; при опытах употребляли смолу КУ-2 с содержанием ДВБ 12 %, но с различным содержанием 5О3Н - групп. [37]
Полагая, что константа г мало изменяется в рассматриваемых системах, отличающихся лишь степенью набухания ионита, приходим к заключению, что экспоненциальный член уравнения ( 8) ( К в уравнении 7) должен зависеть от величины ns ДФ8, которая в свою очередь зависит от степени набухания ионита. Если поглощение ионов сопровождается сжатием ионита ( сорбируется ион, обозначенный индексом 1), то константа К должна уменьшаться при увеличении степени набухания ионита. [39]
Что касается ограниченной роли изменчивости сольватационного фактора, то он был специально изучен в модельной системе, где константа ионного обмена также возрастает с ростом коэффициента набухания ( табл. 3.8) и где было показано не возрастание, а некоторое уменьшение положительного фактора термодинамического потенциала набухания ( в процессе ионного обмена) при увеличении степени набухания ионита. [40]
Различная степень набухания ионообменных смол в воде ( и в водных растворах), зависящая от степени спштости ионита, числа и свойств ионогенных функциональных групп, приводит к различию в проницаемости зерен сорбентов для ионов больших размеров. Повышение степени набухания ионитов вызывает повышенную способность для ионов больших размеров проникать в зерна и поглощаться сорбентами. Емкость сорбции тех же веществ на сильносшитых сорбентах, полученных при введении 10 - 20 % дивинилбензола в смолу, составляет всего лишь миллиграммы на грамм сорбента. Избирательная сорбция инсулина из белковых растворов проводится в колонке, заполненной набухающей сульфосмолой с зернами диаметром 0 2 - 0 5 мм. Медленная диффузия молекул белков в столь большие зерна сорбента не приводит к равновесию даже в течение многих часов. В связи с этим емкость сорбции зависит существенным образом от времени контакта раствора и сорбента. При значительных временах эксперимента сорбентом начинает поглощаться уже заметное количество белков большего молекулярного веса, что ухудшает избирательность сорбции инсулина. [41]
Различная степень набухания ионообменных смол в воде ( и в водных растворах), зависящая от степени сшитости ионита, числа и свойств ионогенных функциональных групп, приводит к различию в проницаемости зерен сорбентов для ионов больших размеров. Повышение степени набухания ионитов вызывает повышенную способность для ионов больших размеров проникать в зерна и поглощаться сорбентами. Емкость сорбции тех же веществ на сильносшитых сорбентах, полученных при введении 10 - 20 % дивинилбензола в смолу, составляет всего лишь миллиграммы на грамм сорбента. Избирательная сорбция инсулина из белковых растворов проводится в колонке, заполненной набухающей сульфосмолой с зернами диаметром 0 2 - 0 5 мм. Медленная диффузия молекул белков в столь большие зерна сорбента не приводит к равновесию даже в течение многих часов. В связи с этим емкость сорбции зависит существенным образом от времени контакта раствора и сорбента. При значительных временах эксперимента сорбентом начинает поглощаться уже заметное количество белков большего молекулярного веса, что ухудшает избирательность сорбции инсулина. [42]
 |
Сорбционная емкость по меди ( Н и коэффициент набухания некоторых комплекситов в водных и этанольных средах ( ССиа 0 05 моль. [43] |
Из экспериментальных данных следует, что из энергетических затрат системы на комплексообразование в фазе ионита основное значение имеют затраты на деформацию полимерной матрицы Ея. При переходе от одного растворителя к другому степень набухания ионита в координационно-активной форме изменяется весьма сильно. Симбатно со степенью набухания изменяется и сорбционная емкость гелевых комплекситов. [44]
Замена на иоиите одного иона другим приводит к изменению степени набухания ионита. При этом некоторое количество растворителя либо проникает в ионит, либо удаляется из него. Введение сильно сольватированного многозарядного иона приводит к уменьшению степени набухания ионита, что связано с уменьшением степени сольватации ионов и ионита в результате их сильного электростатического взаимодействия. Аналогичная картина имеет место и при переводе карбоксильного катионита в водородную форму. Это наблюдается и в том случае, когда поглош. Таким образом, процесс обмена иоисв на сильнонабухающих вонитах с термодинамической точки зрения характеризуется изменением свободной энергии в результате перехода ионсв А из раствора в ионит и ионов Аг в раствор и переноса растворителя из раствора в ионит или из ионита в раствор. [45]
Страницы: 1 2 3 4 5