Степень - обратимость
Cтраница 2
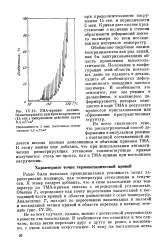 |
ТМА-кривая полиме-тилметакрилата при кратковременном ( 15 сек. импульсном действии груза 6 4 кГ / еж2. [16] |
Кривая дает полное представление о величине и степени обратимости деформаций данного полимера во всем исследованном интервале температур. Обобщенно подобные записи воспринимаются как ряд линий, как бы заштриховывающих область проявления высокоэла-стичности. Положение и конфигурация этой области позволяют, даже не вдаваясь в детали, судить об особенностях деформационного поведения данного полимера. В особенности это относится, как мы увидим в дальнейшем, к полимерам, деформируемость которых изменяется в ходе ТМАв результате процессов кристаллизации или образования пространственных структур. [17]
Уравнение ( 1 - 4) позволяет оценивать степень обратимости ( или, как говорят, степень совершенства) круговых процессов и относить циклы к группе обратимых или необратимых. [18]
Величина / Cs ( или to) характеризует степень обратимости реакции. Чем больше К, тем более обратима электрохимическая реакция. Если потенциал электрода отличается от равновесного на условно принятую величину 50 мВ, реакция считается необратимой. [19]
Таким образом, эксергетический метод позволяет судить о степени обратимости внутренних процессов не по изменению энтропии, а по разности эксергий входящего и выходящего потоков теплоносителя. [20]
Величина ks ( или i) непосредственно характеризует степень обратимости электрохимической реакции. Чем больше ks, тем в более обратимых условиях протекает электрохимическая реакция при прохождении данной величины поляризующего тока. Электрохимические реакции, протекающие при равновесных или практически равновесных потенциалах, называют обратимыми. Если потенциал электрода существенно отличается от равновесного значения, например на 50 - - 100 мв, то говорят о необратимых электрохимических реакциях. [21]
Важно подчеркнуть, что этот метод позволяет судить о степени обратимости процессов внутри аппарата по внешней характеристике - разности эксергий на входе аппарата и на выходе из него. [22]
Из разобранного в предыдущем параграфе примера видно, что степень обратимости процесса увеличивается по мере уменьшения его скорости. Это происходит потому, что необратимость всегда связана с неравновесностью проходимых системой состояний. А неравновесность будет, очевидно, тем меньше, чем меньше скорость процесса по сравнению со скоростью самопроизвольного установления в системе термодинамического равновесия. В предельно медленном процессе все состояния, через которые проходит система, будут просто равновесными, и поэтому такие процессы называют равновесными, или квазистатическими. [23]
Эта зависимость ( в случае ее решения) дает степень обратимости процесса. [24]
Степень обратимости процесса расширения аь так же как и степень обратимости процесса сжатия az, будем считать лри исследовании для всех циклов постоянными. [25]
В подобном случае говорят о термодинамически обратимом процессе, причем степень обратимости тем больше, чем медленнее течет реакция. Разумеется, полная обратимость является идеальным пределом, так как для ее реализации необходима бесконечно малая скорость процесса. Можно показать, что при вполне обратимом течении реакции работа имеет наибольшую величину. [26]
Решая задачу о чувствительности определения, важно знать, какова степень обратимости используемой для определения реакции при принятых условиях поляризации. [27]
 |
Прибор АУ-4М. [28] |
Напряжение, прилагаемое к двум индикаторным электродам, зависит от степени обратимости электродных процессов, в которых участвует реагент и определяемое вещество. Чем больше обратимость системы, тем меньшее напряжение требуется налагать на электроды. [29]
Высота пика Яп на ДИП в меньшей степени зависит от степени обратимости электрохимических реакций, чем на квадратноволновых полярограммах. Поэтому можно было априори предположить, что предварительное электролитическое накопление окажется более эффективным для анализа методом дифферент циальной импульсной полярографии, чем в квадратно-волновой. [30]
Страницы: 1 2 3 4