Степень - окисление - железо
Cтраница 2
На рис. 10 можно видеть, что степень окисления железа достаточно интенсивно растет со временем и за 1 мин. [16]
Основываясь на предыдущих методах, легко произвести определение обеих степеней окисления железа при совместном присутствии. [17]
Как изменяются кислотно-основные свойства гидратов окислов железа с изменениями степени окисления железа. [18]
Железо, его оксиды и гидроксиды, зависимость их свойств от степени окисления железа. Химические реакции, лежащие в основе получения чугуна и стали. [19]
Железо, его оксиды и гидроксиды, зависимость их свойств от степени окисления железа. Химические реакции, на которых основано производство чугуна и стали. [20]
Железо, его оксиды и гидроксиды, зависимость их свойств от степени окисления железа. Химические реакции, на которых основано производство чугуна и стали. [21]
Железо, его оксиды и гидроксиды, зависимость их свойств от степени окисления железа. Химические реакции, на которых основано производство чугуна и стали. [22]
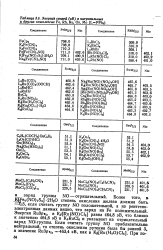 |
Энергия связей ( эВ в нитрозильных и других комплексах Fe, Rh, Ru, Os, Mo ( LPPhs. [23] |
Более того, & J № e4 ( NO) 7S3 ] - 2H2O степень окисления железа должна быть - и 5, если считать группу NO положительной, а из рентгено-электронных данных видно, что заряд на Fe положительный. Энергия Ru3p / 2 в K [ iRu ( NO) Cl5 ] равна 464 8 эВ, что близко-к значению 464 6 эВ в KaRuCle и указывает на отрицательный заряд NOj-группы. [24]
Рассмотрим еще один вопрос: что получается при взаимодействии ионов железа и гексацианоферратов, когда степень окисления железа в них одинакова. Эта соль очень легко окисляется, и поэтому быстро синеет даже на воздухе, превращаясь в берлинскую лазурь. [25]
Главная трудность, которая возникает у абитуриентов при ответе на этот вопрос, состоит в нахождении степени окисления железа в продукте реакции. Здесь следует руководствоваться следующим правилом. [26]
Коэффициенты Ка Кк, ф и Р, зависящие от химического состава воды, свойств взвешенного осадка и степени окисления железа до поступления воды в осветлитель, определяются экспериментальным путем. [27]
Эти катионы необходимо обнаруживать из первоначального раствора, поскольку в ходе анализа при действии ряда групповых реагентов ( H2S, NaOH и Н2О2 и др.) происходит изменение степени окисления железа. [28]
Другими словами, циано-ферри ( 3) ат-ион действует1 и1 как осадитель и как окислитель, и синяя окраска появляется, когда железо находится в катионе в степени окисления, отличной от степени окисления железа, находящегося в анионе. Циано-ферри ( 3) ат-иоя представляет собой сильный окислитель и в щелочном растворе он легко окисляет гидрозакись железа до гидроокиси железа. [29]
Страницы: 1 2 3 4