Степень - окисление - центральный ион
Cтраница 2
Комплексы с центральным ионом, обладающим степенью окисления выше 3, довольно редки. По мере повышения степени окисления центрального иона следует ожидать повышения прочности связи в комплексе. Однако при слишком высокой степени окисления центральный ион настолько сильно притягивает электроны лигандов, что они полностью отрываются от лигандов. В результате комплекс оказывается неустойчивым, а металл восстанавливается, переходя в более низкое состояние окисления. [16]
Для этого иона, введенного в решетку кристалла SrTiO3, A. Она указывает, что при увеличении степени окисления центрального иона увеличивается перенос заряда с лигандов на центральный ион. [17]
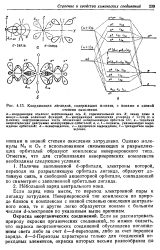 |
Координация лигандов, содержащих я-связи, с ионами в низкой. [18] |
Если заряд иона высок, то переход электронной пары к лиганду затруднен. Невернеровский тип комплексов по природе близок к комплексам с низкой степенью окисления центрального иона, те и другие легко образуются ионами с большим числом d - электронов по указанным выше причинам. [19]
Соль содержит комплексный анион. Вначале называют электроотрицательные, а затем - молекулярные лиганды с окончанием о, как и в предыдущем случае, и с введением в наименование ( если это нужно) греческих числительных. Степень окисления центрального иона ( если это вызывается необходимостью) также отмечается римскими цифрами в скобках теперь уже перед названием элемента. [20]
Соль содержит комплексный анион. Вначале называют электроотрицательные, а затем - молекулярные лиганды с окончанием-о, как и в предыдущем случае, и с введением в наименование ( если это нужно) греческих числительных. Степень окисления центрального иона ( если это необходимо) также отмечается римскими цифрами в скобках теперь уже перед названием элемента. [21]
При наименовании таких соединений вначале указывается название комплексного аниона с сохранением той же последовательности наименования его отдельных составных частей. Название комплексного аниона заканчивается суффиксом - am, после чего в родительном падеже указывается внешнесферный катион. Степень окисления центрального иона указывается римскими цифрами в скобках перед его названием. [22]
Вначале называют комплексный катион, в котором последовательность наименовании отдельных составных частей - - лигандов и центрального иона остается той же. Степень окисления центрального иона указывают после его названия римскими цифрами, взятыми в скобки. Затем указывают название внешнесферного аниона. [23]
 |
Определенные рентгеноспектральным методом заряды атомов в соединениях. [24] |
В таком варианте эффективный заряд характеризует объемное распределение электронной плотности в молекуле. Они хорошо согласуются с величинами, найденными для некоторых элементов рентгенографически. Точность определения эффективных зарядов элемента в разных химических соединениях достаточна, чтобы установить их зависимость от степени окисления центрального иона и от химической природы соседнего атома. [25]
Соль содержит комплексный анион. Вначале называют электроотрицательные, а затем - молекулярные лиганды с окончанием о, как и в предыдущем случае, и с введением в наименование ( если это нужно) греческих числительных. После этого называют комплексообразователь, используя латинское название элемента с прибавлением суффикса - ат. Степень окисления центрального иона ( если это вызывается необходимостью) также отмечается римскими цифрами в скобках теперь уже перед названием элемента. [26]
При наименовании таких соединений вначале указывают внешнесферный катион, после чего следует название комплексного аниона с сохранением той же последовательности наименования его отдельных составных частей. Название комплексного аниона заканчивается суффиксом - ат. Степень окисления центрального иона указывают римскими цифрами в скобках после его названия. [27]
Соль содержит комплексный анион. Вначале называют электроотрицательные, а затем - молекулярные лиганды с окончанием о, как и в предыдущем случае, и с введением в наименование ( если это нужно) греческих числительных. После этого называют комплексо-образователь, используя латинское название элемента с прибавлением суффикса - ат. Степень окисления центрального иона ( если это вызывается необходимостью) также отмечается римскими цифрами в скобках теперь уже перед названием элемента. Число катионов в соли определяется валентностью комплексного аниона и в названии соли не отображается, например: K [ Co43 ( NH3) 2 ( NO2) 4 ] - тетранитро-диам-мин - ( Ш) кобальтат калия. [28]
Затем некоторые из наиболее распространенных названий, такие, как лутео и пурпурео, стали использоваться для обозначения комплексов M ( NH3) 6 и M ( NH3) S C1 безотносительно их цвета. Вернер предложил номенклатуру комплексных соединений, которая с некоторыми изменениями используется до сих пор. По одному из его предложений ( сейчас оно не принято) для указания степени окисления центрального иона использовали суффиксы - а, - о, - и или - е для степени окисления - ( - 1, 2, 3 или - f4 соответственно, например, [ Co ( NH3) e ] Cl - - гексамминкобальтихлорид; KjPtCiJ - тет-рахлороплатоат калия. [29]
Страницы: 1 2