Степень - отравление - катализатор
Cтраница 1
Степень отравления катализатора зависит от природы примеси. Отравляющее влияние тяжелых металлов, повидимому, снижается в последовательности: никель, ванадий, железо, медь, свинец. [1]
Зависимость степени отравления катализатора от количества поглощенного им яда для многих случаев в широких пределах имеет линейный характер. [2]
Для установления зависимости степени отравления катализатора от количества SiF4 в газовой смеси была проведена вторая серия опытов. [3]
Работами многих исследователей показано, что степень отравления катализатора независимо от типа отравления зависит от многих факторов: природы отравляющего металла, типа соединения, в котором металл находится на катализаторе, степени дисперсности металла на поверхности катализатора, количества отложенного металла и возраста отложения, первоначальной активности катализатора и его типа. [4]
Сада и Вен [287] проанализировали влияние степени отравления катализатора на селективность при отравлении пор для сложных реакций трех типов. Рассмотрены реакции на сферической грануле, на бесконечной плоской пластине и бесконечной цилиндрической грануле. Для случая одновременного протекания двух реакций рассмотрено воздействие яда на протекание как одной из них, так и обеих. [5]
Таким образом, скорость гидрирования пропилена за счет перераспределения водорода не зависит от степени отравления катализаторов. [6]
Активность катализаторов зависит от многих причин-от их состава и способа приготовления, от размера зерен и степени их пористости, от срока службы и степени отравления катализатора. Для оценки отравляющего действия на катализатор различных ядов и примесей в газе пользуются показателем, называемым отравляемостью катализатора. [7]
Длительные испытания, проводимые в условиях стационарного слоя катализатора, исключают воздействие некоторых факторов, существующих в промышленных условиях и оказывающих значительное влияние на характер и степень отравления катализатора металлами. В связи с этим в промышленной установке с движущимся слоем катализатора некоторая часть отложенных металлов удаляется в процессе истирания его поверхностного слоя. [8]
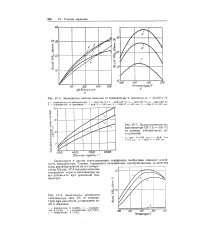
Сероводород и другие серосодержащие соединения необратимо снижают активность катализатора. Степень отравления катализатора пропорциональна количеству серы, адсорбированной на его поверхности. На рис. IV-8 показано влияние содержания серы в катализаторе на его активность при различной температуре. [10]
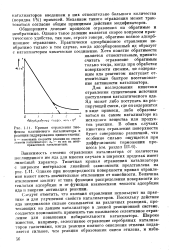 |
Кривая отравления тио-феном платинового катализатора в реакции гидрирования цикпогексена. [11] |
Для исследования кинетики отравления существенен источник поступления каталитического яда. Яд может либо поступать из реагирующей смеси, где он содержится в виде примеси, либо образовываться на самом катализаторе из исходного вещества или продуктов реакции. Зависимость степени отравления катализатора от количества поглощенного им яда для многих случаев в широких пределах имеет линейный характер. Типичная кривая отравления катализатора с широким интервалом линейной зависимости представлена на рис. 1.11. Однако при неоднородности поверхности кривая отравления может иметь значительные отклонения от линейности. Величина отклонения зависит от типа функции распределения поверхности по теплотам адсорбции и от функции взаимосвязи теплоты адсорбции яда и энергии активации реакции. [12]
Исследование влияния сернистых соединений на катализаторы гидрирования показывает [244], что тиоэфиры более токсичны, чем меркаптаны и сероводород, тиофенол - более, чем тиофен, ( 3-этилфенилсульфид занимает промежуточное положение. Указанные ряды токсичности совпадают с изменением донорной способности серы в этих соединениях. Имеющиеся в литературе сведения о независимости степени отравления катализатора от природы сернистых соединений [343, 346] относятся к высокотемпературным процессам. В этом случае, вероятно, сернистое соединение разлагается с выделением сероводорода, который и является контактным ядом. Если скорость элиминирования сероводорода достаточно велика, то можно не заметить различия в действии сернистых соединений разного строения на катализатор. [13]
На рис. 25 показано влияние различных металлов ( никеля, железа, ванадия, меди и свинца) на активность ш закоксовывание катализатора. Авторы считают, что отравляющее действие металлов, цо-видиио у, снижается в последовательности: никель, железо, ванадий, медь, свинец. Другие исследователи считают, что металлы располагаются в таком порядке: никель, медь, железо, ванадий, и даже приводят количественные соотношения силы их водзей-ствия. Как уже отмечалось большинство исследователей при изучении влияния различных металлов на степень отравления катализатора оперировали относительно большим количествами металла, чем их было на промышленном равновесном катализаторе. Видимо потому, что в работе С 57 J опирались На данные о содержании металлов в промышленном катализаторе, определенные ими зависимости отличаются от всех остальных; уравнение для определения активности катализатора имеет следующий Вид: активность. GOJVa O, Следовательно, ванадий существенно увеличивает активность катализатора, коэффициент, перед содержанием железа также взят со знаком плюс. [14]
Исследование восстановления фенилпиридинов [65] показало, что 2 - и 3-фенилпиридины легко восстанавливаются водородом в присутствии окиси платины до 2 - и 3-феншшиперидинов, в то время как 4-фенилпиридин возвращается из реакции в неизмененном состоянии. Дифенилпиридин был восстановлен в тех же самых условиях до 2 6-дициклогексилпиперидина, в то время как из пентафенилпиридина образовался тетрациклогексилпи-перидин-одна молекула бензола отщепляется в результате гидрогенолиза. В общем случае производные пиридина восстанавливаются легче, чем сам пиридин, а вещества с заместителями в положении 2 обычно восстанавливаются с наибольшей легкостью. Так, например, 2-бензилпиридин восстанавливается до 2-бензилпиперидина с 96-процентным выходом при 100, в то время как для пиридина требуется температура примерно 200 с тем же самым катализатором. Изучение скоростей восстановления гомологов пиридина, проведенное М. И. Ушаковым [72, 73], показывает, что восстановление протекает легче в том случае, если в пиридиновое кольцо вводится дополнительная метильная группа; этот эффект выражен тем ярче, чем ближе к атому азота расположен заместитель. Азотистые основания сильно адсорбируются катализаторами гидрирования; возможно, что стерический эффект заместителей, смежных с атомом азота, уменьшает эту сильную адсорбцию и тем самым снижает степень отравления катализатора. [15]
Страницы: 1