Степень - полнота - реакция
Cтраница 3
Таким образом, осли ысходнтле концентрации известны, можно рассчитать степень полноты реакции но достижении равновесия. [31]
Упражнение 11.17 Единичный объем смеси с исходным составом с-0 реагирует до степени полноты реакции t без изменения объема. [32]
Таким образом, АН представляет собой частную производную полной энтальпии по степени полноты реакции. [33]
Отношение х / у не зависит от начального давления бутана и степени полноты реакции при постоянной температуре. При 520 С были сделаны следующие-измерения. [34]
 |
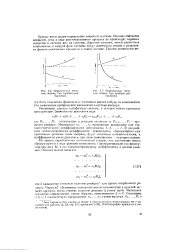
T. 15. Фазовая плоскость при F О И G 0. поэтому СОСТОЯ-единственном стационарном режиме. Ние реактора должно смещаться. [35] |
Когда изображающая состояние реактора точка попадает на линию SU, F О и степень полноты реакции стационарна, но G 0, так что температура продолжает уменьшаться. Направление стрелок показывает, что решение должно закручиваться по спирали вокруг стационарной точки Т; типичное решение дает кривая OPQRS. Эта кривая представляет ход решения нестационарных уравнений в фазовой плоскости, причем время t служит параметром, изменяющимся вдоль кривой. [36]
 |
Шфцна. тьнып моль-тле объемы при крайнем раз. [37] |
Через т обозначены начальные масса компонентов в нулевой момент и ре ми ни, когда степень полноты реакции равна пулю. [38]
 |
Адиабатические пути обратимых экзо - и эндотермической реакций. [39] |
Чтобы вычислить равновесный состав, достигаемый в адиабатических условиях, следует найти изменение температуры со степенью полноты реакции. [40]
После реакционного аппарата содержание органических сернистых соединений снижается примерно до 95 % от начального, причем степень полноты реакции тем выше, чем полнее протекает основная реакция и чем меньше сероводорода в исходном газе. При дальнейшей очистке газа от двуокиси углерода водой под давлением извлекается примерно 80 % остатка. [41]
Следовательно, при условии х д 0 и у у0 термодинамический потенциал 5s представляет собой квадратичную форму от степеней полноты реакций. Так как при этом дополнительном условии термодинамический потенциал имеет минимум, разность 5й - 5 0 всегда положительна и Р есть положительно определенная матрица. [42]
Упражнение 11.26. При постоянном давлении изменение объема реагирующей идеальной газовой смеси вследствие изменений общего числа молей п температуры пропорционально степени полноты реакции. [43]
В, и поэтому концентрации В и С пропорциональны соответственно 1 - и, где, как и прежде, степень полноты реакции - химическая переменная. [44]
В учебниках классической термодинамики показывается, что иногда в уравнении (3.45) можно пренебречь членом, содержащим изменение энтропии в зависимости от степени полноты реакции. [45]
Страницы: 1 2 3 4