Степень - распад
Cтраница 2
Возможность и степень распада на ионы определяется природой растворенного вещества и природой растворителя. Так, при растворении ионных соединений ( поскольку они уже состоят из ионов) имеет место диссоциация. Роль растворителя в этом случае заключается в создании условий для разъединения ионов противоположного знака и в пре-пятствовании процессу молизации. Диссоциация ионных соединений протекает тем легче, чем полярнее молекулы растворителя. [16]
Возможность и степень распада на ионы определяется природой растворенного вещества и природой растворителя. Так, при растворении ионных соединений ( поскольку они уже состоят из ионов) имеет место диссоциация. [17]
Возможность и степень распада на ионы определяется природой растворенного вещества и природой растворителя. Так, пр и растворении ионных соединений ( поскольку они уже состоят из Ионов) имеет место диссоциация. Роль растворителя в этом случае заключается в создании условий для разъединения ионов противоположного знака и в пре-пятствовании процессу молизации. Диссоциация ионных соединений протекает тем легче, чем полярнее молекулы растворителя. [18]
Возможность и степень распада растворенного вещества на ионы определяется природой растворенного вещества и растворителя. Электролитической диссоциации подвергаются ионные соединения и молекулярные соединения с полярным типом связи в полярных растворителях. Вода относится к наиболее сильноионизирующим растворителям. [19]
Возможность и степень распада растворенного вещества на ионы определяется природой растворенного вещества и растворителя. Вода относится к наиболее сильноионизирующим растворителям. [20]
Характер и степень распада молекул гидратной оболочки зависит от природы катионов и анионов - чем сильнее поляризующее действие ионов, тем в большей степени протекает гидролиз. [21]
Характер и степень распада молекул гидратной оболочки зависят от природы катионов и анионов - чем сильнее поляризующее действие ионов, тем в большей степени протекает гидролиз. [22]
С изменением степени распада в диапазоне 29 - 70 % выход метана и этилена возрастает почти в 5 раз, в то же время выход водорода и пропилена увеличивается только в 1 5 раза. При большем давлении и глубине распада ( 180 мм, 76 %) выход этана возрастает более чем в два раза. [23]
В зависимости от степени распада на ионы электролиты делят на сильные и слабые. [24]
У различных комплексных соединений степень распада при диссоциации комплексных ионов различна. Степень распада того или иного комплексного иона может быть выражена через константу равновесия, которую называют константой нестойкости ( или распада) комплекса и обозначают / Сн - Чем больше / Си, тем комплексное соединение менее устойчиво. [25]
 |
Координационные числа некоторых ионов металлов. [26] |
У различных комплексных соединений степень распада при диссоциации комплексных ионов различна. [27]
Под сапробностью принято понимать степень распада органических веществ в загрязненных водах. Организмы, обитающие в загрязненных водах, называют сапробионтами или сапробными организмами. Они могут служить индикаторами ( показателями) загрязнения, или различных ступеней разложения органического вещества в водоеме. Способность организмов обитать в условиях разной степени сапробности объясняется потребностью в органическом питании и выносливостью к вредным веществам, образующимся в процессе разложения органического вещества. [28]
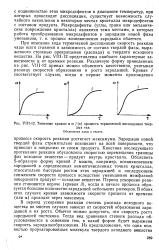 |
Типичные кривые а f ( т процесса термической диссоциации твердых тел. Объяснения даны в тексте. [29] |
В период ускорения реакции степень распада исходного вещества во многих случаях зависит от скоростей образования зародышей и их роста. Обычно можно допустить, что скорость роста зародышей постоянна. Тогда вид уравнения степени распада обусловливается в основном тем, в какой форме будет выражена скорость зародышеобразования. [30]
Страницы: 1 2 3 4