Степень - стабилизация
Cтраница 4
При этом методе исходят из того, что степень стабилизации истечения газа за равные промежутки времени одинакова и кривая q q ( Ар2), построенная по данным, полученным при частичной стабилизации, имеет такую же форму, как и истинная кривая, но сдвинута относительно последней на угол, зависящий от времени стабилизации. [46]
Учет степени гидрофобности аминокислотных остатков дает информацию о степени стабилизации глобулярной макромолекулы белка гидрофобными взаимодействиями. Однако такого рода оценки недостаточны. Необходимо рассматривать реальную структуру глобулы и учитывать весь баланс происходящих в ней взаимодействий. Упрощенная теория Фишера не обеспечивает этого. [47]
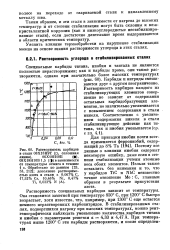
Диаграмма на рис. 64 позволяет судить о влиянии степени стабилизации и возможности ее нарушения при перегреве. Например, сталь со степенью стабилизации 0 38 - 10 - 3, перегретая до 1300 С, будет вести себя примерно так же, как сталь нестабилизированная с 0 05 % С. Рядом с перегретой зоной, как правило, находится зона с температурами, более низкими, чем температуры растворимости карбидов титана или ниобия, и отвечающая температурам стабилизирующего отжига ( см. гл. В случае достаточно длительной выдержки при этих температурах ( минимально необходимое время стабилизирующего отжига тстаб) и соответствующей степени стабилизации сталь этой зоны будет совершенно устойчива к дальнейшим влияниям критических температур, а благодаря этому и к межкристаллитной коррозии. Значение стабилизирующего отжига объясняет следующий пример. [48]
То же самое относится и к сталям с низкой степенью стабилизации. В случае толстостенной заготовки нужно иметь в виду, что и при быстром охлаждении после растворяющего отжига сердцевина ее может находиться при повышенных температурах столько времени, что у нее появится склонность к межкристаллитной коррозии. [49]
Деринг и Гофман [10] привели некоторые количественные данные о степени стабилизации сульфониевой группой соседнего карбаниона. [50]
По результатам измерений при искусственной и естественной стабилизации определяют степень стабилизации приборов. [51]
Протонирующая сила кислот Бренстеда может быть увеличена с увеличением степени стабилизации аниона, образующегося вместе с карбоний-ионом. Это соображение заставляет вспомнить все сказанное выше в разд. Если в качестве кислоты Бренстеда применяется галогеново-дород, то протонодонорные свойства среды могут быть увеличены при добавлении веществ с сильным специфическим сродством к галоген-аниону, например хлористого алюминия. Особенно интенсивно изучены в качестве среды для генерации кар-бониевых ионов такие комбинации, как НС1 - A1CU, НС1 - ВС13 [1018], HF - BF3 [871], HF - SbF5 [967] и FSO3H - SbF5 [974], Они превосходят серную кислоту и по кислотности и по химической инертности. Кроме того; серная кислота замерзает при относительно высокой температуре ( 10 37), а названные кислоты можно использовать при крайне низких температурах, которые необходимы для замедления реакций, приводящих к разрушению неустойчивых карбониевых ионов. Растворы можно разбавлять сернистым ангидридом [967], что облегчает работу при низкой температуре. [52]
Когда анионный центр возникает у атома углерода при тройной связи, степень стабилизации соответствует карбанион-ной. Алкины-1, хотя и не являются сильными кислотами, все же более сильные кислоты, чем алканы. [53]
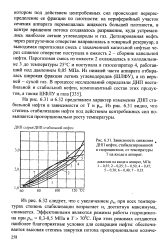 |
Зависимость снижения. [54] |
Из рис. 6.32 следует, что с увеличением рт при всех температурах степень стабилизации возрастает и, достигнув максимума, снижается. Эффективными являются режимы работы гидроциклона при рех 0 3 - 0 5 МПа и Т 70 С. [55]
Поэтому все данные о влиянии ниобия содержат некоторую ошибку, даже если в степени стабилизации учтены атомные веса обоих элементов. Нельзя также оставлять без внимания и то, что у карбидов TiC и NbC неизвестно точное отношение Me: С, главным образом в результате присутствия азота. [57]
 |
Ионизационные потенциалы метилзамещенных радикалов. [58] |
Тем не менее пропорциональная зависимость между а и ионизационным потенциалом показывает, что степень стабилизации при замене водорода на метальную группу зависит от того, какая часть положительного заряда катиона переходит на вновь появившийся атом углерода. [59]
Страницы: 1 2 3 4