Степень - торможение - электродный процесс
Cтраница 1
Степень торможения электродного процесса зависит от величины покрытия электродной поверхности поверхностно-активными продуктами; наиболее значительное торможение наблюдается обычно при покрытиях, близких полному. [1]
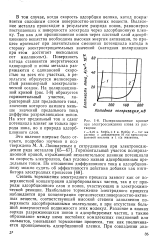 |
Поляризационные кривые при электроосаждении олова из растворов. [2] |
Степень торможения электродного процесса зависит как от поверхностной концентрации адсорбированных частиц, так и от природы адсорбционного слоя и ионов, участвующих в электрохимической реакции. Различие в знаках заряда разряжающихся ионов и адсорбируемых частиц, а также образование между ними нестойких комплексных соединений или сольватов, уменьшают торможение процесса, так как увеличивается проницаемость адсорбционной пленки. [3]
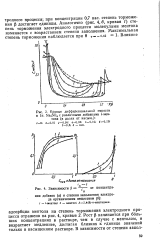 |
Кривые дифференциальной емкости в 1н. Na2SO4 с различными добавками / - ментона ( в долях от насыщ.. [4] |
Аналогично ( рис. 4 6, кривая /) степень торможения электродного процесса молекулами ментона изменяется с возрастанием степени заполнения. [5]
Применение метода непрерывного обновления всей реакционной поверхности твердого металлического электрода под раствором электролита при одновременном исследовании кинетики электродного процесса позволяет дать количественную оценку степени торможения электродного процесса отдельными его ступенями. Торможение электродного процесса от тех ступеней, скорость которых определяется адсорбцией или образованием защитных пленок, устраняется при непрерывном обновлении поверхности электрода. Наоборот, торможени-ступеней, зависящих от процесса передачи зарядов, не снимается при обновле нии поверхности. [6]
Исследование ряда характерных электродных процессов показало, что сопоставление кинетики электродного процесса при наличии или отсутствии непрерывного обновления поверхности металлического электрода позволяет дать количественную оценку степени торможения электродного процесса отдельными его ступенями. Торможение электродного процесса от тех ступеней, скорость которых определяется адсорбцией или образованием защитных пленок, устраняется при непрерывном обновлении поверхности электрода. Наоборот, торможение ступеней, зависящих от процесса передачи зарядов, не снимается при обновлении поверхности. Торможение электродного процесса от диффузионных ограничений ( концентрационная поляризация) также устраняется обновлением поверхности, но в данном случае ( в отличие от адсорбционных ограничений) достаточно и энергичного перемешивания, без механической зачистки поверхности. [7]
Влияние органических ингибиторов на скорость электродных процессов определяется степенью заполнения поверхности электрода молекулами ингибитора. Особый интерес представляет установление зависимости между адсорбируемостью органических веществ, степенью торможения электродного процесса и особенностями строения их молекул. [8]
В молекуле гс-ментадиена неоднородность электрического поля обусловлена в основном наличием сопряженных двойных связей, пространственное разделение разрядов отсутствует. Поэтому только при степенях заполнения поверхности электрода молекулами п-ментадиена 0 0 9 наблюдается заметное увеличение степени торможения электродного процесса в результате возникновения потенциального барьера. Однако, как следует из табл. 3, величина At / при 6 1 значительно меньше, чем в случае с ментолом и ментоном, в связи с этим адсорбция молекул га-ментадиена приводит к небольшому раздвижению потенциалов полуволн ApV2aK знодно-катодных волн и не влияет на снижение предельного тока. [9]
Большой экспериментальный материал, накопленный при исследовании электрохимического поведения металлов, наглядно показывает, что кинетика электроосаждения и растворения металлов тесно связана с адсорбционными явлениями. Чужеродные частицы, присутствующие в электролите или возникающие в процессе электролиза, адсорбируются на поверхности электрода и, как правило, тормозят, а иногда и изменяют характер протекания электрохимических реакций. Степень торможения электродных процессов зависит в основном от прочности связи чужеродных частиц с поверхностью электрода. При рассмотрении кинетики электродных реакций обычно предполагают, что поверхность электрода является однородной, и не учитывают влияния адсорбированных чужеродных частиц на скорость разряда и ионизации металла. Последнее часто приводит к ошибочным трактовкам экспериментальных результатов. [10]
Вторая глава посвящена главным образом электроосаждению цинка. Показано, что не только ионы цинка, но и все другие частицы, находящиеся в приэлектродном слое, оказывают влияние на скорость протекания электродного процесса. В частности, степень торможения электродного процесса, вызываемого адсорбированным водородом, будет различна в зависимости от присутствующих в растворе анионов. [11]
Страницы: 1