Степень - гидролиз - хлор
Cтраница 1
Степень гидролиза хлора в водном растворе увеличивается с повышением температуры и уменьшается с повышением концентрации. В присутствии хлоридов и кислот степень гидролиза хлора существенно уменьшается. При повышении величины рН до 3 и выше хлорная вода практически не содержит молекулярного хлора. [1]
По мере образования этиленхлоргидрина степень гидролиза хлора уменьшается, так как образующаяся соляная кислота сдвигает равновесие реакции ( 11 14) влево. [2]
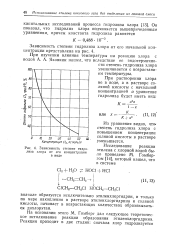 |
Зависимость степени гидролиза хлора от его концентрации в воде. [3] |
Из уравнения видно, что степень гидролиза хлора с повышением концентрации соляной кислоты в растворе уменьшается. [4]
С увеличением концентрации соляной кислоты в растворе степень гидролиза хлора уменьшается; концентрация хлорноватистой кислоты оказывает на гидролиз хлора менее сильное влияние. [5]
 |
Зависимость выхода дихлорэтана от концентрации этиленхлоргидрина в растворе при гипохлорировании концентрированного этилена ( кривая Гомйерга. [6] |
Положительное влияние температуры на выход этиленхлоргидрина обусловливается, по мнению авторов, увеличением скорости и степени гидролиза хлора. Оно проявляется в случае тонкого дробления газов, при котором суммарная величина поверхности пузырьков этилена настолько велика, что перекрывает уменьшение растворимости этилена, имеющее место при повышении температуры. [7]
Другие авторы считали целесообразным применение более высоких температур ( 40 - 50 С), поскольку степень гидролиза хлора по мере повышения температуры возрастает. [9]
Гидролиз хлора был впервые изучен А. А. Яковкиным ( 1863 - 1936), определившим константу равновесия этой реакции и степень гидролиза хлора при различных температурах. [10]
Гидролиз хлора был впервые изучен А. А. Яковкиным ( 1863 - 1936), определившим константу равновесия этой реакции и степень гидролиза хлора при различных температурах. [11]
Эти, а также некоторые другие авторы [14 - 16] нашли, что присутствие в хлорной воде соляной кислоты уменьшает степень гидролиза хлора. Это влияет на скорость реакции этилена с хлором и с хлорноватистой кислотой, а следовательно, и на относительный выход обоих продуктов. [12]
По мнению других исследователей35 37, этиленхлоргидрин образуется в результате взаимодействия этилена с молекулярным хлором, образовавшимся в качестве вторичного продукта из хлорноватистой и соляной кислот, и водой, а степень гидролиза хлора практически не имеет значения для этого процесса. Таким образом, спорным вопросом38 40 является роль гидролиза хлора в реакции образования этиленхлоргидрина. [13]
Процесс гидролиза зндотермичен, теплота гидролиза хлора уменьшается с ростом температуры и при 85 - 95 С равна нулю. С повышением температуры степень гидролиза хлора возрастает. [15]
Страницы: 1 2

