Степень - делокализация - электрон
Cтраница 1
Степень делокализации электрона часто можно определить также по двум другим эффектам. Первый из них связан с тем, что если неспаренные электроны не локализованы на атоме металла, то константа спин-орбитального взаимодействия уменьшается, так что - тензор становится менее анизотропным, чем при отсутствии ковалентной связи. [1]
Исследуя угловую корреляцию в органических жидкостях или кристаллах, можно судить о степени делокализации электронов в структурно сходных сериях. [2]
Такое свойство параметра h обусловлено малостью параметров m и k, характеризующих степень делокализации электронов. Поскольку дело-кализация в насыщенных соединениях выражена слабо, любое изменение энергии орбит серы, вызванное, например, изменением параметра h, даст аддитивную поправку к энергии всей молекулы. [3]
Когда кислотности углеводородов рассматриваются как функций устойчивости нейтральных н анионных форм, особенно в отношении степени делокализации электронов г анноне, необходимо определение кислотности в состоянии равновесия. Мы только что видели, как можно получить такие данные. Однако во многих случаях иметь данные по равновесию нельзя. Для таких ситуаций оказывается возможным определить, какой протон в молекуле отрывается легче всего, илн уста новить - быстрее или медленнее депротонируе. [4]
Все эти образования, в отличие от предыдущих, относятся к системам, которые, помимо участков с низкой степенью делокализации электронов, содержат участки с высокой степенью делокализации. [5]
Радикальная атака обычно происходит по той связи, разрыв которой будет способствовать наибольшей делокализации неспаренного электрона, поэтому существует определенная корреляция между энергией активации реакции замещения и степенью делокализации электрона. Многие реакции радикального замещения осуществляются по цепному механизму. [6]
Окрашенными оказываются также многие твердые вещества с промежуточным типом связи, хотя составляющие их ионы бесцветны в растворах и ионных кристаллах, Это может быть обусловлено некоторой степенью делокализации электронов, рассмотренной выше. Так, например, бромистое серебро и фосфат серебра - бледно-желтого цвета, хотя ионы серебра, бромида и фосфата в растворах бесцветны. Более глубокие окраски наблюдаются при наличии атомов одного и того же элемента в разных состояниях окисления. [7]
Анализ спектров ЭПР этого ряда радикалов показывает, что в первых шести неспаренный электрон находится лишь в одном кольце и влияние его не передается на р-группы, тогда как в остальных радикалах степень делокализации электрона значительно выше. [8]
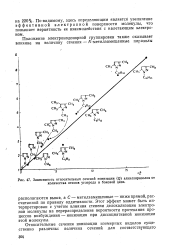 |
Зависимость относительных сечений ионизации ( Q алкилпиразолов от количества атомов углерода в боковой цепи. [9] |
С - метилзамещенные - ниже прямой, рассчитанной по правилу аддитивности. Этот эффект может быть интерпретирован с учетом влияния степени делокализации электронов молекулы на перераспределение вероятности протекания процессов возбуждения - ионизация при диссоциативной ионизации этой молекулы. [10]
Протяженность блоков сопряжения и расстояние между ними зави-сят от метода синтеза полимера с сопряженной системой связей, его химического строения, конформационной устойчивости макромолекул, энергии межмолекулярных взаимодействий и от физической структуры полимера. Все факторы, приводящие к нарушению копланарности, снижают степень делокализации электронов и ухудшают свойства полимеров, обусловленные системой сопряжения. Кристаллизация, если она не связана с изменением конформации молекул и нарушением копланарности, приводит к улучшению в первую очередь полупроводниковых свойств, так как переход электронов от одной молекулы к другой облегчается упорядоченным расположением макромолекул в полимере. [11]
Увеличение электроноакцепторной способности заместителей при полярном сопряжении приводит к уменьшению электронной населенности л-спстемы бензольного кольца. Последнее, в свою очередь, вызывает определенное возрастание степени делокализации электронов неподеленных пар атома фтора при их взаимодействии с л-системой кольца. В табл. 81 показано, что вычисленный порядок л-связи С - F увеличивается симбатно со значением ас - константы заместителя. Уравнение (VII.10) указывает, что при увеличении pc F экранирование F19 должно уменьшаться. [12]
Получение сравнительно низкомолекулярных веществ мы объясняем следующим образом. С ростом полифениленовой цепочки увеличивается стабильность радикала ( бирадикала) вследствие увеличения степени делокализации электронов по цепи сопряжения и веса хиноиднои структуры. В пределе образуется радикал, не способный к дальнейшему росту в условиях данной реакции. [13]
Таким образом, метильная группа рассматривается так же, как галогенный заместитель. Хотя была выбрана определенная ориентация группы СН3 в проведенном рассмотрении, можно показать, что степень делокализации электронов между метильной группой и кольцом не зависит от ориентации группы. [14]
Молекулы выбранного адсорбата ( СО) взаимодействуют с этими центрами по донорно-акцепторному механизму с образованием соединений типа карбоншюв с линейной структурой. Различная координационная ненасыщенность поверхностных атомов способствует образованию нескольких типов связей с молекулами адсорбата, отличающихся степенью делокализации электронов и прочностью. Соответственно в спектре термодесорбции появляется несколько форм адсорбированного оксида углерода. [15]
Страницы: 1 2