Различная степень - окисление
Cтраница 2
Хром в различных степенях окисления образует большое число соединений. Наиболее важными являются II ( хромистая), III ( хромовая) и VI ( хромат) степени; II состояние является основным, III состояние - амфотерным, и VI состояние - кислотным. Коммерческое применение находят главным образом соединения с хромом в VI состоянии, соединения в III состоянии также пользуются некоторым спросом. [16]
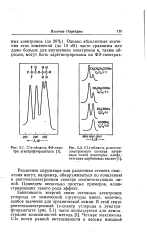 |
Cls-область ФЭ-спек-тра этилтрифторацетата.| Cls-область рентгено-электронного спектра натриевых солей некоторых алифатических карбоновых кислот. [17] |
Различное окружение или различная степень окисления могут, например, обнаруживаться по появлению в рентгеноэлектронном спектре соответствующих лич ний. [18]
Определение ионов ванадия различных степеней окисления при совместном присутствии является насущной задачей, с которой сталкиваются металлурги при получении металлического ванадия. [19]
Соли ванадия в различной степени окисления имеют различную окраску, меняющуюся в зависимости от концентрации и рН среды. [20]
 |
Схема строения молекул V2O5 и HNO3. [21] |
Некоторые свойства оксидов различной степени окисления приведены в табл. 12.20. Данные таблицы показывают, что при повышенных температурах пассивироваться могут только Mb и Та, обладающие тугоплавкими нелетучими оксидами. [22]
 |
Типичные кристаллические решетки металлов. [23] |
Изучение свойств продуктов различных степеней окисления металлов позволяет сделать следующие общие выводы. [24]
Вопрос об устойчивости различных степеней окисления элементов в растворах обсуждался, многими авторами, однако достаточно обоснованные количественные закономерности до сих пор здесь отсутствуют. [25]
Кислоты, соответствующие различным степеням окисления фосфора, проявляют различную восстановительную способность. Так, например, фосфиты восстанавливают йод в щелочной среде, в кислой среде реакция протекает медленно, в то время как восстановление йода гипофосфитами в кислой среде протекает быстро. Характерно их поведение по отношению к растворам медных солей; фосфорноватистая кислота ( гипофосфиты) осаждает из них водородистую медь тогда как фосфористая кислота ( фосфиты) осаждает металлическую медь. [26]
Связь цвета с различными степенями окисления - атома моле-кулы-гостя ( например, серы в ультрамарине) является довольно обычной. [27]
Для элементов с различной степенью окисления возможно образование как катионных многоядерных гидроксокомплексов ( низшие ступени окисления), так и анионных. [28]
Поведение висмута в различных степенях окисления характеризуется данными табл. 1.8. В указанном ряду отчетливо наблюдается усиление металлических признаков простых веществ. Неметаллические модификации висмута неизвестны. [29]
Молибден ( в различных степенях окисления - 0, 2, 3, 4, 5 и 6) входит в состав широкого спектра применяемых в промышленности соединений. Он легко переходит из одной степени окисления в другую при малейших изменениях условий внешней среды. Для этого элемента характерна тенденция к образованию комплексов - за исключением сульфидов и галогенидов, большая часть его соединений представляют собой комплексы. Шестивалентный молибден образует изо - и гетерополярные кислоты. [30]
Страницы: 1 2 3 4