Средняя степень - ассоциация
Cтраница 1
Средняя степень ассоциации % А различных спиртов и фенолов ( по И. [1]
Если средняя степень ассоциации достаточно велика, то отношение трг 2 / трг 1 больше единицы. [2]
Если средняя степень ассоциации р 1, то концентрация мономерных молекул ROH и димеров ( ROH) 2 в спирте невелика. В этих условиях вполне применимо допущение, что константы равновесия и константы скоростей всех реакций ( VIII. В тех случаях, когда р по порядку величины близко к единице, концентрации мономеров и димеров относительно велики. В этих условиях целесообразно выделять реакцию разрыва Н - связи в димерах, потому что изменение энтропии S системы в ходе этой реакции заметно отличается от изменений S в случае более сложных ассоциатов. [3]
Однако средняя степень ассоциации жидкости при температуре кипения, по-видимому, мало отличается от единицы. Данные рентгеноструктурного анализа [15] указывают на квазикристаллический порядок молекул в жидкости. [4]
Так как, в принципе, средняя степень ассоциации р может стремиться к бесконечности, матрицы L и Р должны иметь очень большие размеры. Трудности, возникающие при отыскании собственных значений, при некоторых упрощениях задачи преодолеваются следующим образом. [5]
Из табл. 9 и 10 следует, что средняя степень ассоциации р уменьшается с ростом температуры и увеличением числа атомов углерода в радикале. Для изомерных спиртов ROH величина р уменьшается с увеличением разветвленности радикала и при переходе от первичных спиртов, молекулы которых имеют группу СН2ОН, ко вторичным спиртам, содержащим группу СНОН, и далее к третичным спиртам, с гидро-ксильной группой у третичного атома углерода С - ОН. Если радикал R в молекуле RОН разветвлен, то в ряде случаев [27, 28] на первый план выступают кольцевые и кустообразные ассоциаты. [6]
Знаменатель геометрической прогрессии / С 1 представляет собой функцию средней степени ассоциации р жидкости. [7]
 |
Схема межмолекулярного взаимодействия макромолекул. [8] |
Повышение температуры усиливает тепловое движение макромолекул, что способствует снижению средней степени ассоциации при той же концентрации. Вследствие малой подвижности макромолекул при изменении концентрации или температуры равновесие в растворе устанавливается не сразу, а с течением времени. [9]
Здесь были рассмотрены реакции вида ( VII 1.1) при больших и малых средних степенях ассоциации. [10]
Таким образом, при сопоставлении расчетной и экспериментальной вязкости удается рассчитать среднюю степень ассоциации молекул дайной жидкости, которая служит критерием оценки степени отклонения данной жидкости от состояния молекулярного раствора. Оценка склонности углеводородов нефти к ассоциации в широком интервале температур возможна путем соответствующих элементарных расчетов на основе исследования их вязкостно-температурных свойств [40] и может служить классификационным признаком отнесения исследуемого углеводорода к сильно -, средне - и слабоассоциирующпм жидкостям в определенном диапазоне температур. [11]
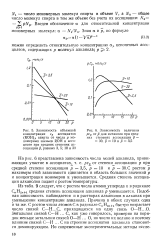 |
Зависимость объемной концентрации ср ассоциатов ( ROH p спирта от числа р мономерных звеньев ROH в ассо-циате при средних степенях ассоциации р, равных 3, 5. 10 и 30.| Зависимость величины. [12] |
Из табл. 9 следует, что с ростом числа атомов углерода п в радикале СпН2п 1 средняя степень ассоциации алканола р уменьшается. Подобная зависимость наблюдается и в растворах алканолов в алканах при уменьшении концентрации алканола. Причина в обоих случаях одна и та же. С на строение ассоциатов алканола становится доминирующим. [13]
Например, в случае идеальных ассоциированных растворов такая связь может быть выражена [5] достаточно точно через среднюю степень ассоциации и другие параметры, характерные для этой модели, дающие вклад в избыточный мольный термодинамический потенциал Гиббса GE, зная который можно вычислить флуктуации мольной доли. [14]
В предположении, что в системе происходит полное связьшание спирта в ассоциаты [ ROH ] 0 a [ ROHJ [ ROH2 ], где [ ROH ] 0 - концентрация спирта; а - средняя степень ассоциации. [15]
Страницы: 1 2