Наиболее устойчивая степень - окисление
Cтраница 2
Простые вещества актиноидов химически активны. На воздухе большинство из них постепенно окисляется кислородом и азотом. При сгорании металлов в кислороде образуются соединения, соответствующие наиболее устойчивым степеням окисления актиноидов. [16]
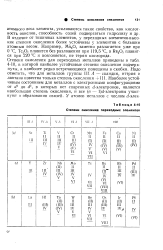 |
Степени окисления переходных элементов. [17] |
В отличие от типичных элементов, у переходных элементов высокие степени окисления более устойчивы у элементов с большим атомным весом. Например, Мп2О7 заметно разлагается уже при О С, Тс2О7 плавится без разложения при 119 5 С, a Re2O7 плавится при 220 С и возгоняется, не теряя кислорода. Степени окисления для переходных металлов приведены в табл. 4 - 10, в которой наиболее устойчивые степени окисления подчеркнуты, а наиболее редко встречающиеся помещены в скобки. Надо отметить, что для металлов группы III Л - скандия, иттрия и лантана известна только степень окисления III. [18]
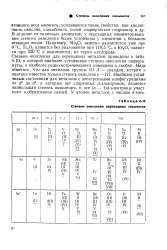 |
Степени окисления переходных элементов. [19] |
Свойства, как кислотность окислов, способность солей подвергаться гидролизу и др. В отличие от типичных элементов, у переходных элементов высокие степени окисления более устойчивы у элементов с большим атомным весом. Например, Мп2О7 заметно разлагается уже при О С, Тс2О7 плавится без разложения при 119 5 С, a Re2O7 плавится при 220 С и возгоняется, не теряя кислорода. Степени окисления для переходных металлов приведены в табл. 4 - 10, в которой наиболее устойчивые степени окисления подчеркнуты, а наиболее редко встречающиеся помещены в скобки. Надо отметить, что для металлов группы III Л - скандия, иттрия и лантана известна только степень окисления - fill. Наиболее устойчивым состоянием для металлов с электронными конфигурациями от d1 до if, в которых нет спаренных d - электронов, является наибольшая степень окисления, и все ( п - 1) - электроны участвуют в образовании связей. [20]
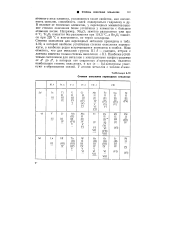 |
Степени окисления переходных элементов. [21] |
В отличие от типичных элементов, у переходных элементов высокие степени окисления более устойчивы у элементов с большим атомным весом. Например, Мп2О7 заметно разлагается уже при О С, Тс2О7 плавится без разложения при 119 5 С, a Re2O7 плавится при 220 С и возгоняется, не теряя кислорода. Степени окисления для переходных металлов приведены в табл. 4 - 10, в которой наиболее устойчивые степени окисления подчеркнуты, а наиболее редко встречающиеся помещены в скобки. Наиболее устойчивым состоянием для металлов с электронными конфигурациями от dl до db, в которых нет спаренных d - электронов, является наибольшая степень окисления, и все ( п - 1) а ( - электроны участвуют в образовании связей. [22]
Степень окисления 3 не характерна для тория и протактиния, мало устойчива для урана и нептуния, легко переходит в 4 для плутония. Начиная с америция степень окисления 3 является наиболее устойчивой. В табл. 15.2 сопоставлены степени - окисления актиноидов и лантаноидов, жирным шрифтом выделены наиболее устойчивые степени окисления. Степени окисления, которые осуществляются только в твердой фазе, взяты в скобки. [23]
Точно так же как лантаноиды образуют ряд родственных элементов, расположенных после La, для которых типичны ионы М3, содержащие от 1 до 14 4 / - электронов, можно было бы ожидать, что и ряд актиноидов включает 14 элементов, следующих за своим прототипом Ас ( который, подобно La, по праву хозяина занимает место в III группе); дополнительные 1 - М4 электронов в актиноидах предпочитают размещаться в оболочке 5 /, а не в оболочке Gd. Однако на самом деле у Th нет 5 / - электропов, а их количество у Ра точно неизвестно, и по своим свойствам эти два элемента являются в гораздо большей степени представителями IV и V групп ( соответственно), чем соответствующие лантаноиды Се и Рг. Так, например, химия тория по существу ограничивается химией Th ( IV), тогда как для церия в основном распространены соединения Се ( III), для Се ( IV) в твердом состоянии известны лишь два бинарных соединения, оксид и фторид. В противоположность Ра с наиболее устойчивой степенью окисления V соединения Pr ( V) вообще неизвестны. [24]
Относительно многих степеней окисления переходных элементов можно с уверенностью сказать только то, что самая низкая общая для них степень окисления, за исключением группы III А, равна 11, а самая высокая равна номеру группы. Это следует из общей электронной структуры ( п - l) d ns2 или ( п - l) dx lnsl, где ( х 2) - номер группы. У переходных элементов с увеличением степени окисления, а в пределах одной группы с увеличением атомного веса элемента усиливаются такие свойства, как кислотность окислов, способность солей подвергаться гидролизу и др. В отличие от типичных элементов, у переходных элементов высокие степени окисления более устойчивы у элементов с большим атомным весом. Например, Мп2О7 заметно разлагается уже при 0 С, Тс2О7 плавится без разложения при 119 5 С, a Re2C7 плавится при 220 С и возгоняется, не теряя кислород. Степени окисления для переходных металлов приведены в табл. 4 - 10; наиболее устойчивые степени окисления подчеркнуты, а наиболее редко встречающиеся помещены в скобки. [25]
Страницы: 1 2