Термодинамическая степень - свобода
Cтраница 3
Надо заметить, что рассматриваемая нами теперь система, состоящая из двух компонент и имеющая две фазы, обладает двумя термодинамическими степенями свободы. Поэтому из четырех величин Р, Т, Ci, ц только две можно выбрать произвольно; если мы выберем, например, Р или Т и одну из концентраций, то другая концентрация будет при этом определена. [31]
Не все параметры состояния равновесных систем являются взаимно независимыми величинами, причем число независимых параметров состояния системы всегда равно числу ее термодинамических степеней свободы. При этом все остальные параметры также приобретают вполне определенные значения, являясь физическими функциями независимых параметров. [32]
Разность между общим числом независимых параметров, которые определяют состояние системы и числом уравнений, связывающих химические потенциалы, называют числом термодинамических степеней свободы или вариантностью системы. [33]
В системе, состоящей из т компонентов, критическая фаза, которая не сосуществует с остальными фазами, имеет т - 1 термодинамических степеней свободы. [34]
Параметры системы, находящейся в состоянии термодинамического равновесия, связаны между собой, причем число независимых параметров состояния системы всегда равно числу ее термодинамических степеней свободы. Например, состояние термодинамической системы, в которой могут изменяться температура и объем ( термодеформационная система), всегда определено, если заданы только два параметра. При этом остальные параметры принимают вполне определенные значения. [35]
Согласно правилу фаз, для однокомпонентной системы равновесие между кристаллической и аморфной фазами при Тт возможно при условии, что система обладает одной термодинамической степенью свободы. Это означает, что каждому значению одной из термодинамических переменных ( например, давлению Р) отвечает лишь одно значение температуры двухфазного равновесия кристалл - расплав. [36]
Указанная выше универсальность кинетической картины фазового перехода проявляется, если предположить, что поведение системы определяется не только параметром порядка, но и другой термодинамической степенью свободы 5, характерное время релаксации TS которой соизмеримо с соответствующим значением тп для параметра порядка. В этой связи в работе [13] предложен еще один механизм проявления принципа Ле-Шателье - за счет нагревания области, прилегающей к выделению 4 фазы, образованному в результате резкого охлаждения системы ниже точки фазового перехода первого рода. При этом роль управляющего па - раметра 5 играет локальное значение температуры в области выделений фазы. Исследование их фазового портрета т) ( 8) и вида самих временных зависимостей ij ( t), S ( t) показывает, что все фазовые траектории разбиваются на два участка. На первом величины т /, 5 сравнительно быстро эволюционируют со временем, и он не сказывается существенным образом на кинетическом поведении системы. Оно представляется медленным изменением величин ri ( t), S ( t) на втором участке, положение которого определяется близостью к сепаратрисе и образно обозначено в [13] как русло большой реки. [37]
Уравнение (102.2) называется правилом фаз или законом равновесия фаз: в равновесной термодинамической системе, на которую из-внешних факторов оказывают влияние только температура и давление, число термодинамических степеней свободы равно числу компонентов минус число фаз плюс два. [38]
Уравнение (102.2) называется правилом фаз или законом равновесия фаз: в равновесной термодинамической системе, на которую из внешних факторов оказывают влияние только температура и давление, число термодинамических степеней свободы равно числу компонентов минус число фаз плюс два. [39]
Температура системы изменяется в таких пределах, что каждое вещество может разлагаться. Сколько термодинамических степеней свободы имеет данная система. Что представляет собой равновесная система. [40]
Наличие набора условий, сопровождающих установление равновесия в гетерогенной системе позволяет решить вопрос о числе термодинамических степеней свободы, которыми обладают многофазные многокомпонентные системы. Под термодинамической степенью свободы понимают независимый термодинамический параметр равновесной системы, изменение которого в определенных пределах приводит к изменению химического потенциала одного или более компонентов и не вызывает исчезновения одних и образования других фаз или компонентов. [41]
Систему определяют четыре основных параметра: температура, давление и концентрации воздуха в каждой из двух фаз растворителя. Такая система имеет две термодинамические степени свободы, т.е. только два параметра могут быть изменены без нарушения равновесия. Это означает также, что, например, при заданных температуре и концентрации воздуха в газовой фазе другие параметры ( давление и концентрация воздуха в жидкой фазе) определяются расчетом. Температура задается из условия требуемой глубины химической реакции, а давление выбирается таким образом, чтобы количество растворенного кислорода было достаточным для окисления органических веществ до требуемой величины. Как правило, количественные величины параметров определяются экспериментально. [42]
По числу термодинамических степеней свободы различают: безвариантную термодинамическую систему, у которой число степеней свободы равно нулю; одно -, двух - или трехвариантные системы, у которых число степеней свободы соответственно равно единице, двум или трем. Система, у которой число термодинамических степеней свободы больше трех, называется многовариантной. [43]
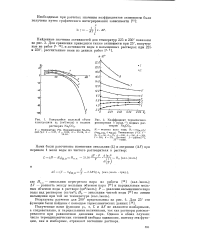 |
Кажущийся мольный объем [ IMAGE ] Коэффициент термического электролита ру ( см3 / моль в водных расширения а ( град. 1 водных рас. [44] |
Полученные нами функции yY, a, L и А61 не являются изобарными, а следовательно, и парциальными величинами, так как растворы рассматриваются при равновесном давлении пара. Однако в обоих случаях число термодинамических степеней свободы одинаково, поэтому эти функции, как и изобарные, отражают состояние раствора. [45]
Страницы: 1 2 3 4