Обычная степень - окисление
Cтраница 1
Обычные степени окисления для этих элементов легко предсказать на основании их электронной конфигурации, имея в виду два общих принципа. [1]
Обычные степени окисления для этих элементов легко предсказать на основании их электронной конфигурации. [2]
Данные таблицы относятся к обычным степеням окисления. [3]
Даже для ионов металлов в обычных степенях окисления иногда наблюдаются изменения порядка положения лигандов, непосредственных или близких соседей в ряду. [4]
 |
Стереохимия As, Sb и Bi. [5] |
Помимо соединений, в которых висмут существует в обычных степенях окисления III и V, этот металл образует также субгалогениды, а также многоядерные катионы и анионы, в которых имеются связи металл - металл. В структурах BiBr [8] и обеих кристаллических модификациях Bil [9] осуществляется цепочечный мотив, в котором атомы Bi связываются двумя совершенно различными способами. [6]
Элементы, у которых не указана степень окисления, осаждаются в обычной степени окисления. [7]
Она с успехом применяется к большому числу комплексов переходных металлов в обычных степенях окисления, где величины перекрываний электронных облаков не слишком велики. В тех же комплексах, где перекрывание существенно, методы ТКП и ТПЛ непригодны. [8]
Она с успехом применяется к большому числу комплексов переходных металлов в обычных степенях окисления, где величины перекрывания электронных облаков не слишком велики. В тех же комплексах, где перекрывание существенно, методы ТКП и ТПЛ непригодны. [9]
В электрохимических исследованиях дипиридильных комплексов было обнаружено, что металл в исходном деполяризаторе имел обычную степень окисления II или III. [10]
Постояннотоковые полярограммы дипиридильных комплексов типа [ М ( Dipy) 3 ] ( C104) n в ацетонитриле на фоне перхлоратов натрия и тетраэтиламмония ( с обычной степенью окисления центрального атома в исходном деполяризаторе) содержат до шести ступеней, из которых первые три или четыре, в зависимости от природы центрального атома [ MFe ( II), Fe ( III), Cr ( III), Co ( II), Co ( III), Mn ( II) ], являются одноэлектронными и в сумме соответствуют переносу ( п 1) электронов ( в соответствии с уравнением Ильковича), а две последние обусловлены разрядом частиц лиганда. [11]
Изучение строения и свойств кристаллических тел, получившее сильное развитие в последнее время, выявило, в частности, что наряду с соединениями, в которых элементы проявляют обычные степени окисления, существует довольно много соединений, не отвечающих им, которые называют соединениями нестехиометриче-ского состава. Так, соединение состава FeO является неустойчивым в обычных условиях и вместо него реально существует соединение состава Рео. Причины таких соотношений могут быть различными. В приведенном примере они связаны с более высокой концентрацией вакансий атомов железа, чем вакансий атомов кислорода при обычном в атмосферных условиях парциальном давлении кислорода в воздухе. [12]
Изучение строения и свойств кристаллических тел, получившее сильное развитие в последнее время, выявило, в частности, что наряду с соединениями, в которых элементы проявляют обычные степени окисления, существует довольно много соединений, не отвечающих им, которые называют соединениями нестехиометриче-ского состава. О, которое устойчиво в кристаллическом состоянии. Причины таких соотношений могут быть различными. В приведенном примере они связаны с более высокой концентрацией ваканский атомов железа, чем вакансий атомов кислорода при обычном в атмосферных условиях парциальном давлении кислорода в воздухе. [13]
Изучение строения и свойств кристаллических тел, получившее сильное развитие в последнее время, выявило, в частности, что наряду с соединениями, в которых элементы проявляют обычные степени окисления, существует довольно много соединений, не отвечающих им / которые называют соединениями нестехиометриче-ского состава. Так, соединение состава FeO является неустойчивым в обычных условиях и вместо него реально существует соединение состава Рео 94тО, которое устойчиво в кристаллическом состоянии. Причины таких соотношений могут быть различными. В приведенном примере они связаны с более высокой концентра - - цией вакансий атомов железа, чем вакансий атомов кислорода при обычном в атмосферных условиях парциальном давлении лсис-лорода в воздухе. [14]
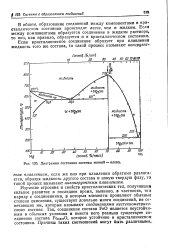 |
Диаграмма состояния системы магний - олово. [15] |
Страницы: 1 2