Стереохимия - соединение - углерод
Cтраница 1
Стереохимия соединений углерода исключительно разнообразна. Простые С-С и кратные СС, СС связи углерод - углерод в различных комбинациях образуют линейные и разветвленные цепи или замыкаются в кольца. [1]
Поэтому стереохимия соединений углерода будет рассмотрена более подробно, чем стереохимия других элементов. [2]
Современные представления о стереохимии соединений углерода будут рассмотрены позднее, в соответствующих разделах книги. [3]
Современные представления о стереохимии соединений углерода будут рассмотрены позднее, в соответствующих разделах книги. [4]
Кроме успешного объяснения стереохимии соединений углерода, теория валентных связей также успешно объяснила строение координационных соединений. В этом случае обычно необходимо принимать во внимание влияние d - орбиталей. Наиболее часто получаются & р2 - гибридные связи, обусловливающие плоскую квадратную структуру, и oT3sp3 - гибридные связи, приводящие к октаэдру. [5]
Кроме успешного объяснения стереохимии соединений углерода, теория валентных связей также успешно объяснила строение координационных соединений. В этом случае обычно необходимо принимать во внимание влияние d - орбиталей. Наиболее часто получаются с ( 5р2 - гибридные связи, обусловливающие плоскую квадратную структуру, и d2sp3 - гибридные связи, приводящие к октаэдру. [6]
 |
Относительная прочность и угловое распределение связывающих орбиталей. [7] |
Кроме успешного объяснения стереохимии соединений углерода теория валентных связей также успешно объяснила строение координационных соединений. В этом случае обычно необходимо принимать во внимание влияние d - орбиталей. [8]
Кроме успешного объяснения стереохимии соединений углерода, теория валентных связей также успешно объяснила строение координационных соединений. В этом случае обычно необходимо принимать во внимание влияние d - орбиталей. Наиболее часто получаются Й5р2 - гибридные связи, обусловливающие плоскую квадратную структуру, и cPsp3 - гибридные связи, приводящие к октаэдру. [9]
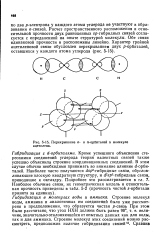 |
Перекрывание а - и л-орбиталей в молекуле ацетилена. [10] |
Кроме успешного объяснения стереохимии соединений углерода теория валентных связей также успешно объяснила строение координационных соединений. В этом случае обычно необходимо принимать во внимание влияние d - орби-талей. Наиболее часто получаются й р2 - гибридные связи, обусловливающие плоскую квадратную структуру, и й ( 25р3 - гибридные связи, приводящие к октаэдру. [11]
По аналогии со стереохимией соединений углерода, азота и других элементов можно было ожидать, что если молекулы аммиака, радикалы или ионы расположены вокруг центрального атома металла ( Go, Pt, Ni, Си, Сг, Fe, Os и др.) в пространстве, то должна наблюдаться структурная и пространственная изомерия. [12]
За последние пять лет было опубликовано несколько книг но стереохимии и конформационному анализу, в том числе монографии Илиела Стереохимия соединений углерода и Илиела, Аллинжера, Энжиала и Моррисона Конформационный анализ. Появление этих книг было вызвано высоким уровнем исследовательской активности в области стереохимии, что, в свою очередь, способствовало проведению еще более широких исследований. В результате эти книги в некоторых деталях оказались устаревшими, хотя они до сих пор служат хорошим пособием для изучения основных концепций стереохимии или конформацион-ного анализа. [13]
Теоретические основы и методический подход к расчетам такого рода неоднократно уже обсуждался и излагался в научной литературе ( см., например, монографию Илиела Стереохимия соединений углерода, гл. [14]
Асимметричные четвертичные фосфониевые соли типа R1R2R3R4PX ( IV) t в которых все группы R различны, могут быть разделены на оптические изомеры, что указывает на сходство стереохимии этих соединений со стереохимией соединений четырехковалентного углерода и четвертичных аммониевых солей. [15]
Страницы: 1 2