Стехиометрия - взаимодействие
Cтраница 1
Стехиометрия взаимодействия между титрантом и определяемым компонентом - другое важное условие использования реакции в объемном анализе - может быть нарушена, если в системе возможно протекание и индуцированных реакций. Таковыми являются реакции, которые в измеримой степени протекают в системе под влиянием другого взаимодействия. Например, окисление SOs иодом до SO2i одновременно индуцирует окисление SOl - кислородом воздуха; при окислении иодида ванадатом так же происходит окисление I - кислородом воздуха. Типичный для перманганатометрии пример индуцированной реакции наблюдается при титровании Fe ( II) MnOI в присутствии хлоридов. [1]
Стехиометрия взаимодействия между хемосорбированным кислородом и газообразным водородом, как и стехиометрия обратной реакции между хемосорбированным водородом и газообразным кислородом, зависит от природы металла и от температуры. [2]
Уравнения связи различны для каждого из случаев стехиометрии взаимодействия в жидкой фазе. [3]
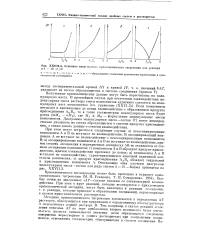 |
Основные типы кривых криоскопического титрования для реакции. [4] |
Особые точки на диаграммах AT-состав связаны со стехиометрией взаимодействия. [5]
Следует еще раз подчеркнуть, что хотя метод расчета / С для каждого из случаев стехиометрии взаимодействия является совершенно строгим, точность определения константы равновесия соответствующего процесса зависит от того, насколько величина Ay ( N искажена неидеальностью соответствующей исходной системы А-В. [6]
Поскольку максимум г в таких системах в основном приходится на состав образующегося в системе соединения [19, 530], минимум на изотерме к, в свою очередь, также может свидетельствовать о стехиометрии взаимодействия. [8]
При не очень больших константах равновесия это приближение является достаточным даже в тех случаях, когда на основании этих зависимостей рассчитывают выход реакции ( см. ниже); для определения же стехиометрии взаимодействия это приближение оказывается достаточным почти всегда. [10]
Поскольку максимум т в таких системах в основном приходится на состав образующегося в системе соединения [19, 530], минимум на изотерме - л, в свою очередь, также может свидетельствовать о стехиометрии взаимодействия. [12]
Диаграммы Дсц и Д 3 ( отклонение экспериментальных величин температурных коэффициентов от значений этих свойств, рассчитанных в предположении отсутствия взаимодействия) в системах с взаимодействием характеризуются экстремумами, приходящимися на область стехиометрии взаимодействия, что также может быть использовано для целей физико-химического анализа. [13]
Сопоставление изотерм парциальных молярных свойств, относящихся к смесям с взаимодействием и к смесям, где после смешения произошло изменение ассоциативного состояния компонентов, но не произошло взаимодействия, является весьма чувствительным методом установления факта и стехиометрии взаимодействия в квазидвойной системе. [14]
Вот почему диэлькометрия в приложении к системам, не содержащих ассоциированных компонентов, может считаться весьма чувствительным методом физико-химического анализа, в то время как в случае ассоциации одного или обоих компонентов диэлькометрия пока не может дать определенных сведений о стехиометрии взаимодействия. [15]
Страницы: 1 2