Стехиометрия - соединение
Cтраница 2
Преимуществом получения иитерметаллических соединений пиролизом комплексных гидридов по сравнению с непосредственным сплавлением металлов является возможность достижения большей чистоты препаратов и более точного выполнения стехиометрии соединений, так как все исходные вещества - LiAlH4, Се ( АШ4) 3, Ni ( NH3) e ( BH4) 2 и другие - получаются обменными реакциями в растворах и подвергаются перекристаллизации в жидких органических растворителях. В то же время при прямом сплавлении металлов для получения интерметаллического соединения всегда возможен угар компонентов за счет улетучивания, взаимодействия с материалом тигля или обменной реакции с флюсом. [16]
При столь высоких температурах образуются зерна больших размеров и критическая плотность тока оказывается низкой, а из-за потерь алюминия за счет испарения трудно выдержать точную стехиометрию соединения. К тому же термообработка катушек при таких температурах оказывается сложной технической проблемой. Для этого соединения пока еще не найдена технология, эквивалентная получению Nb3Sn с применением бронзы. [17]
 |
Фаза р системы Pb - Na. [18] |
С другой стороны, хорошо изучены металлические фазы, где состав химического соединения, судя по характеру изотерм состав - свойство, находится в пределах данной фазы и, следовательно, некоторая неупорядоченность, безусловно, является следствием не только избыточно прибавленных против стехиометрии соединения компонентов, но и каких-либо глубоких превращений самого соединения, совершающихся без разрыва однородности фазы. [19]
Ионное легирование полупроводниковых соединений интересно прежде всего с точки зрения введения примесей при пониженных температурах, когда значительно уменьшена или практически исключена вероятность образования тепловых дефектов. Появляется также возможность сохранить стехиометрию соединения в отличие, например, от легирования диффузией примесей, когда изменение состава в той или иной мере неизбежно. [20]
Медь содержит один s - электрон вне заполненной Зй. Если исключить формальную аналогию в стехиометрии соединений одновалентной меди и соединений щелочных металлов, то между ними очень мало общего. Заполненная rf - оболочка значительно менее эффективно экранирует s - электрон от заряда ядра, чем замкнутая электронная конфигурация инертного газа. [21]
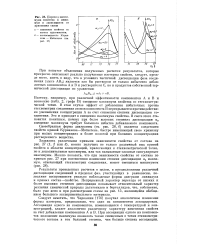 |
Переход максимума свойства в минимум в зависимости от уравнения связи. [22] |
Поэтому, например, при различной эффективности компонентов А и В и возможно ( табл. 2, графа 15) смещение максимума свойства со стехиометри-ческой точки. В этом случае эффект от добавления избыточных против стехиометрии соединения атомов компонента В перекрывается противодействием уменьшения концентрации А за счет снижения степени диссоциации соединения. Это и приводит к смещению максимума свойства. В свете этого становится понятным, почему при более высоких степенях диссоциации сс0 смещение максимума требует большого избытка добавляемого компонента. Своеобразная форма диаграммы ( см. рис. 28, 6) является следствием свойств кривой Курнакова-Матиссена, быстро изменяющей свою кривизну при малых концентрациях и более пологой при больших концентрациях растворенного вещества. [23]
 |
Изотермы выхода, по Н. И. Степанову, для соединений АВ ( а и АВ2 ( 6. [24] |
Вычислив форму изотерм выхода соединений АВ [166] и АВ2 [169] и задаваясь величиной выхода при стехиометрическом отношении компонентов, Степанов получил форму кривой выхода. Им было доказано, что максимальный выход всегда отвечает стехиометрии соединения и в случае, если К оо, выход выражается двумя прямыми, пересекающимися под острым углом. При любом конечном значении К выход выражается уже кривой с максимумом, тем более пологим, чем меньше значение К. [25]
При термическом испарении обычно используется трехтемпера-турный метод, при котором независимо задаются температуры подложки и двух испарителей, содержащих соответственно металл и халькоген. Температуру испарителей выбирают так, чтобы в паровой фазе концентрация обоих компонентов соответствовала стехиометрии соединения. [26]
Ванадий можно рассматривать как элемент V группы в той же мере, в какой Ti относится к IV группе. Но в целом его сходство с элементами подгрулпы фосфора мало и проявляется в основном в стехиометрии соединений. Оксо-анионы ванадия и ванадаты не похожи на фосфаты. [27]
Таким образом, уравнение ( 13) в той или иной форме использует для расчета парциальных давлений знание состава конденсированной фазы. Работы, в которых для определения состава пара привлекались сведения о составе азеотропа [116], о конгруэнтной сублимации и стехиометрии соединений [117, 126, 127], дают примеры применения - уравнения ( 13) на частных случаях. Естественно, что брутто-свойство не чувствительно к тем составляющим, которые слабо представлены в паре. Поэтому не следует ожидать, что уравнение ( 13) может оказаться полезным при определении парциальных давлений молекул, содержание которых не превышает нескольких процентов. В этих случаях приходится пользоваться оценками сечений ионизации. [28]
Наибольший интерес для практического применения в анализе представляют, пожалуй, методы ионометрического определения состава многокомпонентных смесей без их предварительного разделения с одним ионоселективным электродом. Определение в этой группе методов выполняется с привлечением хорошо известного в аналитической химии арсенала средств, позволяющих изменять условные константы комплексообразования близких по свойствам ионов, менять валентное состояние одного из ионов и тем самым нивелировать его метающее влияние или использовать групповой реагент, но учитывать различие в стехиометрии соединений, образуемых с - пим реагентом присутствующими в анализируемой смеси ионами. Анализ становится возможным, если ввести комплексообразователи, связывающие в прочные комплексы метающие ионы, выбрать интервал рН, при котором электрод селективен к определенному иону многокомпонентной смеси, подобрать титрант, который образует комплексы различной прочности или продукты реакции, отличающиеся по своей растворимости, и провести дифференцированное титрование. [29]
Для главных подгрупп системы в химии s - и р-элементов участие d - и / - электронов достаточно характерно. Это связано с возбуждением Зр-электронов при образовании соединений до Sd-состояний и Зр, Sd-гибридизацией. Движение сверху вниз в системе приводит к нарастанию координационных чисел, связанному с увеличением числа а-связей в результате все большего вхождения сначала р -, а затем d - и / - состояний в состав внешнего слоя электронов, что и меняет формулы и стехиометрию соединений. [30]
Страницы: 1 2 3