Стимулирование - коррозия
Cтраница 1
Стимулирование коррозии катодным осадком было подтверждено в лабораторных условиях прямыми гравиметрическими измерениями. Три из них были помещены в осадок из нефтесборного трубопровода Самотлорского месторождения, который удерживался на поверхности образца капроновой сеткой. [1]
Рассмотрим случаи стимулирования коррозии или катодного процесса под влиянием хемосорбирующихся ПАВ молекулярного типа. Типичным примером этого служит действие ацетиленовых соединений при коррозии4 железа или никеля. Несмотря на вероятность протонирования ацетиленовых спиртов, вкладом в возможное участие в разряде прото-нированной формы ПАВ можно пренебречь, так как с ростом концентрации ПАВ этот вклад должен был бы возрастать - и при высоких концентрациях ацетиленовые ПАВ не могли бы. В связи с этим основной вклад в суммарную скорость процесса вносит реакция на поверхности, свободной от адсорбированных частиц ПАВ. [2]
Важную роль в стимулировании коррозии в кислых электролитах приписывают сероводороду, который, вызывая образование на поверхности металла островков из сульфида железа, обусловливает функционирование большого числа местных гальванических элементов. [3]
Предполагается, что механизм стимулирования коррозии суль-фато-восстанавливающими бактериями сводится к какому-то деполяризующему действию. [4]
Затруднения, связанные с образованием осадков и стимулированием коррозии в системах башенного охлаждения, вызываются двумя основными группами организмов - слизью и водорослями. Поскольку их действие проявляется различно, они будут рассматриваться раздельно. В этих системах иногда обнаруживается действие и сульфато-восстанавливающих бактерий, на которых мы также кратко остановимся. [5]
К недостаткам хроматов следует отнести их токсичность, стимулирование коррозии при недостаточной концентрации, необходимость независимого поддержания рН, чувствительность к органическим загрязнениям. [6]
Так как в кислых средах защитные пленки на ряде металлов ( в том числе и на железе) менее стойки, то стимулирование коррозии действием кислорода проявляется тем сильнее, чем меньше значение рН для данного раствора. Наоборот в щелочных растворах даже небольшое количество кислорода может замедлить процессы коррозии. [7]
Температура плавления ванадата натрия составляет 630 С и менее, и поэтому он опасен как по условиям шлакования, так и по условиям стимулирования коррозии. Окислы низших валентностей ванадия тугоплавки. Пяти-окись ванадия имеет температуру плавления 670 С. Надежных данных о наличии в шлаке ванадия низших валентностей не опубликовано. [8]
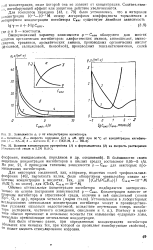 |
Зависимости р, v от концентрации ингибитора.| Влияние концентрации уротропина ( / и формальдегида ( 2 на скорость растворения. [9] |
Как было отмечено ранее, при определенных концентрациях ингибитора ( больших или меньших тех, при которой он проявляет ингибирующие свойства), н может вызвать стимулирование коррозии. [10]
Учитывая, что в объеме раствора могут находиться одновременно все продукты, предусмотренные схемами ( 5.5 - 5.8), можно считать, что все эти продукты в определенной мере ответственны за ингибирование или стимулирование коррозии. Так, расчет характеристик в системе железо - серная кислота - тиомочевина показал [125], что в адсорбционном слое могут находиться как адсорбированные катионы, так и молекулы. В последнем случае адсорбция идет за счет донорно-акцепторного взаимодействия. [11]
Сопоставление зависимостей потенциал ( без наложения тока) - время и скорость коррозии - время в течение длительного периода наблюдений показали, что имеется определенного типа взаимосвязь между этими кривыми, обуславливаемая торможением или стимулированием коррозии вследствие торможения или стимулирования катодного или анодного процесса. [12]
В рассматриваемом случае стимулирование коррозии наблюдается при значительно большем содержании ингибитора. [13]
Однако независимо от того, протекает ли разрушение металла по механизму щелевой коррозии или оно идет в тонких слоях, общим закономерным явлением в рассматриваемом случае является изменение в тонких слоях характера коррозионной среды: более быстрое, чем в объеме насыщение ее продуктами коррозии, образование на поверхности металла осадков - катодных включений, повышение рН среды. Эти изменения в составе среды могут иметь различные последствия, зависящие от того, какой механизм определяет стимулирование коррозии в двухфазных системах. [14]
 |
Образцы, контактировавшие в течение. [15] |
Страницы: 1 2