Изменение - отношение - концентрация
Cтраница 1
Изменение отношения концентрации ( активности) окислителя к восстановителю изменяет величину окислительно-восстановительного потенциала системы. [1]
Другими словами, изменение отношения концентраций ( активности) окислителя и восстановителя приводит к изменению величины окислительно-восстановительного потенциала ред-окс-системы. В том случае, когда активности всех веществ, участвующих в реакции, равны единице, потенциал системы равен стандартному нормальному окислительно-восстановительному потенциалу. [2]
Так как стерео-дифференцирующая способность реагента или катализатора проявляется в изменении отношения концентраций образующихся энантиомеров или диастереомеров, то изучение стерео-дифференцирующих реакций требует особых методов исследования, которыми не располагает синтетическая органическая химия. Чтобы получить надежные экспериментальные данные и выяснить механизм процесса дифференциации, важно уметь владеть основными экспериментальными методами и методами анализа, пригодными для изучения стерео-дифференцирующих реакций. [3]
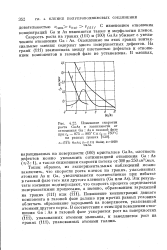 |
Изменение скорости роста GaAs в зависимости от отношения Ga. As в газовой фазе при и 875 - 885 С и п 780 С на разных гранях. [4] |
У ( 100) i ( 111) v iy С изменением отношения концентраций Ga и As изменяется также и морфология пленок. Скорость роста на гранях ( 111) и ( 100) GaAs убывает с увеличением отношения Ga: As. Осажденные на этих гранях эпитак-сиальные пленки содержат много поверхностных дефектов. На грани ( 111) взаимосвязь между плотностью дефектов и отношением компонентов в газовой фазе не установлена. [5]
При значительных изменениях температуры спаев коэффициент а в уравнении (10.6) несколько изменяется, что можно объяснить изменением отношения концентраций электронов oi / o2 в спаянных металлах. [6]
Таким образом, система дыхательного контроля в митохондриях определяет скорость У2 окисления пищевого субстрата в зависимости от изменения отношения концентраций АДФ и АТФ, т.е. движущей силы Х сопряженного процесса. При этом очевидно, что при q поддержание в организме даже небольшой, но постоянной ( стационарной) концентрации АТФ требует отличной от нуля скорости окисления пищевого субстрата. [7]
Вследствие того, что метод не претендует на точность большую 15 - 20 % от измеряемой величины, можно пренебречь изменением отношений концентраций редкоземельных элементов при обогащении проб. [8]
В реакции (8.4) образуются два непарных кислорода, а в реакции (8.6) два непарных кислорода исчезают, в то время как в реакциях (8.5) и (8.3) концентрации непарного кислорода остаются неизменными, хотя происходит изменение отношения концентраций О и Оз. После захода Солнца концентрации атомарного кислорода на высотах ниже примерно 40 км быстро уменьшаются из-за прекращения действия его источников, описываемых реакциями (8.4) и (8.5), а процессы его исчезновения, подчиняющиеся реакциям (8.3) и (8.6), остаются. Поэтому ночью озон не образуется и не разрушается, а суточные изменения концентрации О3 малы на этих высотах. Выше в атмосфере суточные изменения более выражены, так как в дневное время фотолиз Оз протекает быстрее, чем преобразование О назад в Оз, из-за более низкого давления. Заметим, что скорость реакции (8.3) пропорциональна квадрату величины давления. [9]
В зависимости от вида и интенсивности окраски обеих форм отношение Их концентраций, определяющее окраску раствора, может изменяться для различных индикаторов в различных пределах. Легко вычислить, что изменение отношения концентраций от 1: 10 до 10: 1 связано со стократным изменением концентрации Н30, что соответствует изменению рН на две единицы. Приводимый для различных индикаторов интервал изменения окраски, т.е. область, в которой наблюдается смешанная окраска, обычно несколько уже. Это свидетельствует о том, что человеческий глаз обычно малочувствителен. [10]
При использовании отдельных изотопов в качестве меченых атомов для химических и биологических работ нас интересует главным образом не абсолютная величина отношения концентраций изотопов, а изменение этого отношения; при разбавлении обогащенного материала в результате опыта мы интересуемся тем, каков избыток меченых изотопов в материале над их нормальным содержанием. Таким образом, практически значительно важнее получить воспроизводимые значения изменения отношения концентраций изотопов, чем наивысшую точность в значении абсолютной величины этого отношения. Пользуясь стандартным образцом и сравнивая все экспериментально полученные отношения концентраций с их значением для стандарта, автоматически устраняют многие из перечисленных выше ошибок. В литературе [1 ] имеются примеры еще более точных измерений. Единственным элементом ( из всех обсуждаемых в данной статье), анализ которого выполняется обычно с меньшей точностью, является водород. Несколько большая точность может быть получена, если интервал исследуемых концентраций невелик. [11]
К титруемому раствору добавляют раствор индикатора в количестве 1 - 2 капель, и тогда устанавливается определенное соотношение между концентрациями окисленной и восстановленной форм индикатора при заданном окислительном потенциале раствора, который приобретает соответствующую окраску. В процессе титрования этого раствора величина окислительного потенциала меняется, что вызывает изменение отношения концентраций окисленной и восстановленной форм индикатора. Как и в случае индикаторов нейтрализации, не всякое изменение этого отношения может воспринять наш глаз. [12]
С увеличение относительного содержания ионов никеля В ЭЛеК-тролите доля тока, приходящегося на разряд этих ионов, возрастает. Из таблицы видно, что при одной и той же катодной плотности тока изменение отношения концентрации ионов в электролите изменяет величины парциальных токов никеля и кобальта и, следовательно, состав каждого осадка. [13]
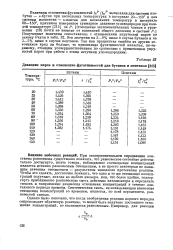 |
Давление паров и отношение фугативностей для бутанов и пентанов. [14] |
При экспериментальном определении константы равновесия существенно показать, что равновесное состояние действительно достигнуто, иначе говоря, наблюдаемое соотношение концентраций является истинно равновесным отношением, а не просто некоторым не имеющим значения отношением - результатом неполного протекания реакции. Чтобы это сделать, достаточно показать, что одно и то же отношение концентраций получают, исходя из любого изомера, или, что более удобно, подвергнуть приближенно равновесную смесь действию катализатора и определить степень и направление изменения отношения концентраций в течение длительного периода времени. Синтетическая смесь, не показывающая изменение отношения концентраций со временем, является, но всей вероятности, равновесной смесью. [15]
Страницы: 1 2