Коррозионная стойкость - железо
Cтраница 1
Коррозионная стойкость железа сильно повышается при легировании его хромом [1-4], и именно таким путем были созданы важные для промышленности нержавеющие стали. [1]
Коррозионная стойкость железа в воде без доступа кислорода воздуха объясняется образованием малорастворимого гидрата закиси железа белого цвета. Последний при взаимодействии с кислородом в присутствии воды легко окисляется, образуя бурый гидрат окиси железа, который также, мало растворим в воде. Далее гидрат окиси железа превращается в сложные гидратиро-ванные окислы железа - ржавчину. В пресной воде скорость коррозии зависит от содержания кислорода, концентрации водородных ионов; более высок ая концентрация кислорода и водородных ионов способствует усилению коррозии. В морской воде при полном погружении скорость коррозии достигает 0 127 мм / год; при наличии в морской воде различных загрязнений скорость коррозии резко возрастает. [2]
Коррозионная стойкость железа зависит от его чистоты. [3]
Исследуют коррозионную стойкость железа, низколегированной, хромистой и хромоникелевой стали, никеля, алюминия, цинка, меди, латуни. [4]
Исследуют коррозионную стойкость железа, низколегированной, хромистой и хоомоникелевой стали, никеля, алюминия, цинка, меди, латуни. [5]
В азотной кислоте коррозионная стойкость железа и сталей выше - от 0 05 до 2 0 мм / год; в кипящем растворе она достигает 5 - 10 мм / год. Меньшую коррозионную активность имеет также фосфорная кислота. Однако при повышенном содержании углерода ( более 0 06 %) в стали скорость коррозии может достигать 3 - 6 мм / год. [6]
Добавки никеля повышают коррозионную стойкость железа и стали в щелочных растворах. [7]
Анализ литературных материалов по коррозионной стойкости железа, меди, алюминия и их сплавов в дистиллер-ной жидкости позволяет утверждать, что железо обладает слабой коррозионной стойкостью. Продукты коррозии железа имеют различный состав, зависящий от условий, в которых протекает коррозия: Fe ( OH) 3, Fe ( ОН), Fe3O4, Fe3O4 H2O и др. Добавка в железо хрома, никеля и ряда других металлов позволяет повысить коррозионную устойчивость этих сплавов в дистиллер ной жидкости. [8]
Насыщение хромом позволяет значительно увеличить коррозионную стойкость железа и стали в азотной и уксусной кислотах, в среде перекиси водорода и в растворе хлористого натрия. Насыщение вольфрамом и молибденом сообщает коррозионную стойкость железу и стали в серной кислоте, насыщение марганцем увеличивает стойкость в среде перекиси водорода и хлористого натрия, а насыщение ниобием и ванадием способствует повышению коррозионной стойкости стали в серной кислоте. [9]
С ростом рН от 9 до 13 коррозионная стойкость железа и сталей повышается, что обусловлено образованием на их поверхности нерастворимых соединений, защищающих металл от воздействия среды. [10]
 |
Зависимость скорости коррозии металлов от рН среды. [11] |
Следует отметить, что при рН14 образуются растворимые ферриты ( NaFeO2) и гипоферриты железа ( Na2FeO2) и коррозионная стойкость железа сильно падает. [12]
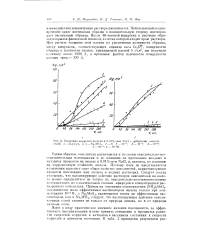 |
Кинетика коррозии железа в 0 01 % - ном NaCl с добавками окислителей а - К Г г2Ог и и - Na.. W04. i - 0. 2 - Ю-5. 3 - 10 - 4. 4 - Ю-3. [13] |
Таким образом, окислители различаются и по своим окислительно-восстановительным потенциалам и по влиянию на протекание анодных и катодных процессов на железе в 0 01 % - ном NaCI, и, наконец, по влиянию на коррозионную стойкость железа. Поэтому пока не представляется возможным выделить одно общее свойство окислителей, характеризующее процессы пассивации ими железа в водных растворах. Следует всегда учитывать, что пассивирующее действие растворов окислителей на железо может определяться не только их окислительно-восстановительными потенциалами, но в значительной степени природой и концентрацией растворенного окислителя. Причем на основании сопоставления ( NH4) 2Mo04, оказавшегося мало эффективным пассиватором железа только при концентрации 10 - 3М, с Na2Mo04, являющимся таким же эффективным пассиватором, как и Na2W04, следует, что пассивирующее действие окислительных солей зависит не только от природы аниона, но и от природы катиона соли. [14]
Действительно, изобарные потенциалы образования оксидов хрома и алюминия - 1059 кДж / моль для Сг2О3, - 1582 кДж / моль для А12О3) намного ниже, чем у оксида железа ( - 740 кДж / моль для Р Оз), однако коррозионная стойкость железа часто оказывается значительно ниже, чем хрома или алюминия. [15]
Страницы: 1 2