Коррозионная стойкость - никель
Cтраница 1
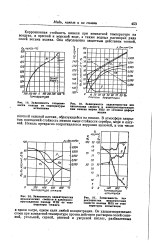 |
Зависимость характеристик неэ ханических свойств и электросопротивления никеля марки НП2 от степени дефора мации.| Зависимость характеристик.| Зависимость хаа. [1] |
Коррозионная стойкость никеля при комнатной температуре на воздухе, в пресной и морской воде, а также водных растворах ряда солей весьма велика. [2]
Повышение коррозионной стойкости никеля в этом случае объясняется известной теорией анодной пассивности. [3]
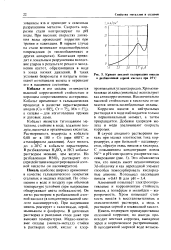 |
Кривая анодной поляризации ннкели в разбавленной серной кислоте при 25 С. [4] |
Алюминий повышает электросопротивление и коррозионную стойкость никеля, а вольфрам и молибден - жаропрочность. Хром повышает стойкость никеля в восстановительных и окислительных растворах, а медь в растворах серной и плавиковой кислот. [5]
По-видимому, возникновение прожогов вызывается плохой коррозионной стойкостью никеля при малых анодных потенциалах ( порядка 0 2 в) и низкой концентрации щелочи. [6]
В концентрированных водных растворах и расплавах щелочей коррозионная стойкость никеля высокая. [7]
Стандартный электродный потенциал никеля ( № 2 - г 2е -) равен - 0 25 В. Коррозионная стойкость никеля объясняется его способностью пассивироваться во многих средах. Никель характеризуется сравнительно высокой коррозионной стойкостью, прочностью, тугоплавкостью, пластичностью и способностью подвергаться различным видам механической обработки. [8]
Нормальный электродный потенциал никеля для процесса Ni - - Ni2 2e равен - 0 25 в. Коррозионная стойкость никеля объясняется его способностью пассивироваться во многих средах. [9]
Углерод повышает прочность никеля при растяжении, предел текучести, твердость и унрочняемость в холодном состоянии. При содержании более 0 02 % углерод снижает коррозионную стойкость никеля в расплавленных щелочах. [10]
С коррозионная стойкость алюминия н железа в парах фенола резко снижается. Технологические примеси в феноле ( например сера) значительно снижают коррозионную стойкость никеля и некоторых марок сталей. [11]
На рис. 2.22 показана кривая для никеля в 0 5 М HjSOj [10], иллюстрирующая основные особенности анодного поведения металла, представляющие интерес с точки зрения его коррозионной стойкости. Возможность пассивации не предсказывается равновесной диаграммой потенциал - рН, однако именно пассивация является одной из причин того, что на практике коррозионная стойкость никеля в кислых растворах оказывается лучше, чем это следует из рассмотрения условий термодинамического равновесия. Вторая и, возможно, более важная причина связана с тем, что активная область ( ЛВС) при анодной поляризации никеля значительно больше, чем при анодной поляризации многих других металлов. Этот факт, а также то, что в электрохимическом ряду никель лишь слегка отрицателен по отношению к равновесию Н / Н2, означает, что на практике скорость растворения никеля в кислых растворах будет небольшой в отсутствие более сильных окислителей, чем Н, или веществ, способных ускорять кинетику анодной реакции. [13]
Хром образует с никелем твердые растворы в широком интервале концентраций ( фиг. Хром в сильной степени повышает жаропрочность и жаростойкость никеля. В значительной мере хром улучшает коррозионную стойкость никеля, особенно в окислителях, содержащих кислород. [14]
Хром образует с нике-яем твердые растворы в широком интервале концентраций ( фиг. Хром в сильной степени повышает жаропрочность и жаростойкость никеля. В значительной мере хром улучшает коррозионную стойкость никеля, особенно в окислителях, содержащих кислород. [15]
Страницы: 1 2
