Стремление - атом - углерод
Cтраница 1
Стремление атомов углерода 1 - 7 - Т и 4 - 8 - 8, связанных одинарными связями, расположиться под тетраэдрическим утлом в - 109, деформирует бензольное кольцо так, что атомы углерода 1 4 оказываются смещенными из плоскости бензольного кольца. Такие молекулы называются пространственнонапряженными. [2]
Стремление атомов углерода переходить в тетрагональное состояние проявляется в многочисленных реакциях цикланонов. Образование циангидринов и восстановление бороводородами идет более чем в тысячу раз быстрее с циклогексаноном, чем с циклодекано-ном. [3]
 |
Иллюстрация к деформации бензольного ядра. Молекула.| Деформация атомом хлора. [4] |
Стремление атомов углерода 1 - 7 - Т и 4 - 8 - 6, связанных одинарными связями, расположиться под тетраэдрическим углом в - 109, деформирует бензольное кольцо так, что атомы углерода /, 4 оказываются смещенными из плоскости бензольного кольца. [5]
Поскольку стремление электроположительного атома углерода восполнять недостаток электронов больше, чем стремление электроотрицательного атома азота отдавать избыток электронов, нитрилы обладают преимущественно электрофильной реакционной способностью. Однако в CN-rpynne имеются неподеленная электронная пара, а также электронодонорные я-связи, поэтому нитрилы проявляют и нуклеофильные свойства. [6]
Что касается стремления атомов углерода концентрировать свои влияния, то мне кажется, что стремление это находится в связи со свойствами углерода как элемента. Являясь в нескольких аллотропических видоизменениях, углерод во всех случаях обладает большой частицей. Сложность частицы, как принимают, зависит от способности атомов углерода к полимеризации, развитой в них в чрезвычайно большой степени. Способность эта сохраняется в атомах углерода и тогда, когда они входят в состав соединений, и от нее зависит все разнообразие и сложность соединений углерода. Если же представить себе атомы углерода в частицах углеводородов тяготеющими друг к другу и допустить, что атомы водорода, соединенные с углеродами, также оказывают взаимное влияние, то станет понятна как причина, так и направление всех вышеприведенных изомеризации. В самом деле, возвращаясь к случаю изомеризации дипропаргила в диметилдиацетилен, как наиболее типичному, мы видим, что в частице дипропаргила как углеродные влияния, так и водородные являются разрозненными, чем и обусловливается сравнительная неустойчивость частицы, в частице же диметилдиацетилена те и другие сконцентрированы. В результате мы имеем группу центральных углеродных атомов, удовлетворивших своему стремлению к полимеризации, а дальнейшей полимеризации, которая обусловила бы распадение частицы и выделение угля, препятствуют дружно соединенные усилия атомов водорода, образовавших метильные группы с двумя периферическими углеродными атомами. [7]
В данном случае стремление атома углерода создать на внешнем электронном уровне устойчивый октет электронов может, по-видимому, удовлетвориться внутри самой молекулы за счет одной из неподеленных пар р-электронов атома кислорода, входящего в эту же молекулу. [8]
Эти отклонения создают внутри молекулы напряжение, которое будет выражаться в стремлении атомов углерода перейти в нормальное, устойчивое состояние, свойственное простой связи. Напряжение это пропорционально углу отклонения, величина которого меняется в зависимости от кратности связи. [9]
Изомерный процесс здесь может обусловливаться или известным присущим атомам брома стремлением занять третичное положение, или стремлением атомов углерода принять более устойчивую группировку, или же, наконец, он может быть следствием обеих причин. Что первая не является здесь ни исключительной, ни даже доминирующей, видно ий данных, касающихся изомерных превращений циклических бромгидринов. [10]
Значительная полярность нитрильной группы обусловливает ее способность к реакциям присоединения. Ввиду того что стремление электроположительного атома углерода восполнять недостаток электронов больше, чем стремление электроотрицательного атома азота отдавать избыток электронов, нитрилы обладают преимущественно электрофильной реакционной способностью. Так как нитриль-ная группа обладает ярко выраженными электроноакцепторными свойствами, она активирует связанные с нею СН2 - гр. [11]
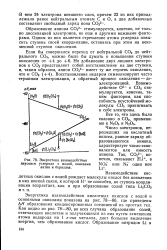 |
Энергетика взаимодействия двуокиси углерода с водой, окислами. [12] |
Образование аниона СО32 - стимулируется, конечно, не только диссипацией электронов, но еще и другими важными факторами. Одним из них является стремление атома углерода повысить ступень своей координации, оставаясь при этом на неизменной ступени окисления. [13]
Карбены являются одними из наиболее энергичных химических реагентов в органической ХИМЕШ. Теплота образования карбена высока и составляет 330 кДж / моль. Несмотря на то что карбен не имеет заряда, он является исключительно активной электрофильной частицей. Это обусловлено стремлением атома углерода достроить свою электронную оболочку до октета. [14]
Карбены являются одними из наиболее энергичных химических реагентов в органической химии. Теплота образования карбена высока и составляет 330 кДж / моль. Несмотря на то что карбен не имеет заряда, он является исключительно активной электрофильной частицей. Это обусловлено стремлением атома углерода достроить свою электронную оболочку до октета. [15]
Страницы: 1