Изменение - валентность
Cтраница 3
В связи с изменением валентности существует два рода солей меди - окионые и за кксные. [31]
Окислительно-восстановительные реакции характеризуются изменением валентности отдельных атомов или групп атомов. [32]
В первой реакции происходит изменение валентности меди и азота, чего не наблюдается во второй. [33]
В колонке Реакция даны изменения валентности частиц для отдельных волн. Эти изменения относятся к атомам или ионам элементов, образующих ядро частицы, активной на электроде. [34]
 |
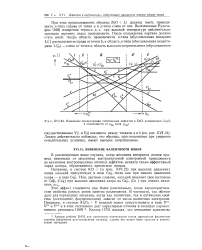
Изменение валентности Ni в решетке NiO под влиянием одно - и трехвалентных катионов. [35] |
На рис. 61 показано изменение валентности никеля в решетке закиси никеля под влиянием одно - и трехвалентных катионов. Электропроводность для этих систем изменяется на 4 - 6 порядков. Ранее считалось, что добавки необратимо закреплены в твердом теле. Однако применительно к модифицирующим металлоидным добавкам, вводимым в металлы и окислы, такое представление слишком категорично, так как ряд исследователей наблюдал перемещение их в твердом теле. [36]
 |
Изменение концентрации собственных дефектов в ZnO, насыщенном Li2O. [37] |
Авторы работы [169] для изменения валентности ионов применяли физические способы ( облучение рентгеновскими лучами), однако это может быть сделано и химическими методами. [38]
 |
Схема прибора для измерения окислительного потенциала. [39] |
Окислительный потенциал для реакций изменения валентности имеет такое же значение, как произведение растворимости для процессов образования и растворения осадков или константы диссоциации кислот и оснований для кислотно-основных процессов. [40]
При отсутствии прямых доказательств изменения валентности или участия в реакции промежуточных соединений типа свободных радикалов полезно дать обзор данных о реакциях ионизированного железа в подобных системах, а затем проанализировать возможность осуществления подобных механизмов в реакциях гемопротеинов. [41]
Процесс образования соли сопровождается изменением валентности азота от 3 до 5, причем пятая связь полярна. [42]
Процесс образования соли сопровождается изменением валентности азота от трех до пяти, причем пятивалентный атом становится полярным. Ион водорода присоединяется к паре электронов атома азота с образованием неполярной связи и, таким образом, содержащая азот группа приобретает положительный заряд. Ионный заряд связан со всей группой в целом, и все четыре валентности азота используются на образование неполярных связей, тогда как пятая - полярная. [43]
Многие химические реакции характеризуются изменением валентности компонентов реакции. С точки зрения электронной теории строения атома такие реакции мы называем окислительно-восстановительными реакциями. [44]
Он основан тоже на изменении валентности меди, которая в данном случае применяется в виде олеата. [45]
Страницы: 1 2 3 4