Строение - льд
Cтраница 1
Строение льда, как и геометрию молекулы воды, мы уже неоднократно обсуждали. [1]
Особым свойством строения льда I является подвижность атомов водорода в его кристаллической решетке, которая беспрерывно изменяется под влиянием внешних воздействий ( изменений отрицательной температуры, давления и пр. При понижении температуры подвижность атомов водорода уменьшается, и лед принимает более упорядоченную ( более плотную и более прочную) структуру, а при температуре - 78 С кристаллическая решетка льда принимает стабильное состояние ( по Савельеву Б. А.); при температуре ниже - 70 С лед из гексагональной сингонии переходит в кубическую. С повышением температуры возрастает энергия активизации его молекул и ускоренная их перегруппировка с ослаблением межмолекулярных связей, что существенно сказывается на снижении прочностных свойств льда. [2]
В вон росе о строении льда, несмотря на большое количество исследований, ясности нет, что связано с трудностями, вызываемыми спецификой объекта. [3]
В пределах севера Русской равнины повторно-жильные льды имеют эпигенетическое происхождение, о чем свидетельствует конфигурация жил и строение льда. Начало их образования обычно связывают с историческим похолоданием. В то же время некоторые исследователи отмечают возможность и современного роста повторно-жильных льдов. Однако в целом жилы льда находятся в законсервированном состоянии. [4]
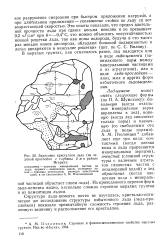 |
Зарисовка кристаллов льда ( из ле - Я14ригтЬ1л / г ножной PTDVK-дяной прослойки с глубины 2мв районе ячеистыи ( СЛОЖНОЙ струк. [5] |
Структура льда-цемента почти не изучалась, кристалло-опти-ческое же исследование структуры избыточного льда ( льда-прослойков) показало чрезвычайную сложность строения льда, различную величину и расположение его кристаллов. [6]
Структура воды имеет очень большое значение, так как это среда, в которой протекают важнейшие химические процессы, включая химию жизни. Строение льда интересно как ключ к пониманию структуры воды. Известно девять модификаций льда, устойчивость которых зависит от температуры и давления. Лед, образующийся в равновесии с водой при 0 С и давлении 1 атм, называют лед-I. [7]
Ряд солей кристаллизуется из раствора в форме кристаллогидратов: N32804 - 10Н2О, Na2COs - 10Н2О, Na2B4O7 10H2O, являющихся по своей структуре тектогидратами. Тектогидраты имеют строение льда, в полостях которого равномерно расположены противоположно заряженные ионы. [8]
Ряд солей кристаллизуется из раствора в форме кристаллогидратов: Na2SO4 10Н2О, Na2CO3 10Н2О, Na2B4O7 10Н2О, являющихся по своей структуре тектогидратами. Тектогидраты имеют строение льда, в полостях которого равномерно расположены противоположно заряженные ионы. [9]
На примере строения льда 1 мы видели, что основные модели, не расходясь в вопросе о положении кислорода, опирались на различные вспомогательные соображения для характеристики позиций водорода, давая разные решения задачи. [10]
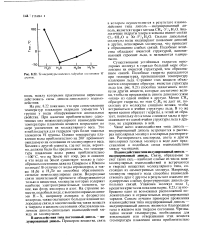 |
Температуры кипения гидридов элементов VI группы. [11] |
Сильно дипольные молекулы воды индуцируют появление диполей в других, неполярных молекулах, что приводит к образованию слабых связей. Подобные вещества обладают ячеистой структурой, напоминающей строение льда, и называются клатра-тами. [12]
Этим и можно объяснить трудную сжимаемость воды; в природных условиях она сжимается главным образом под действием адсорбционных сил, испытывая на поверхности раздела фаз колоссальное давление, превышающее 3 - 3 5 тыс. МПа. По своим свойствам адсорбционная ( прочносвязанная) вода приближается к твердому ( псевдокристаллическому) телу, строение которого, однако, резко отличается от строения льда и характеризуется высокой степенью упорядоченности. [13]
Таким образом, Пруппахер считает обязательным условием проявления влияния электрического поля на кристаллизацию воды присутствие твердого тела. Механизм этого влияния заключается, согласно Пруппахеру, в том, что под действием больших зарядов, которые образуются на поверхности твердого тела при разрыве поверхности жидкости, в ней возникают комплексы молекул, соответствующие строению льда и играющие роль ядер кристаллизации. [14]
Минерал содержит около 45 % воды и устойчив при температуре ниже 0 15 С. При более высокой температуре гидрогалит плавится: его кристаллы и агрегаты сходны с кристаллами и агрегатами льда. Решетка гидрогалита отражает в какой-то мере деформированное строение льда. Расстояние между частицами Н2О в структуре льда равно 0 276 нм. В такой ажурной постройке почти 2 / 3 пространства свободно от атомов. [15]
Страницы: 1 2