Строение - полученный углеводород
Cтраница 1
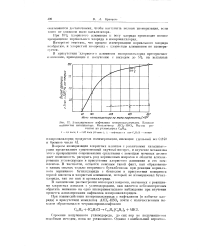 |
Алкшшрованио нафталина пзопропилхлоридом. Влияние количества катализатора. Катализатор A1C12 - HSO4. Выход рассчитан на углеводород С22Н32. [1] |
Строение полученного углеводорода, до сих пор не получавшегося подобным методом, пока не установлено. [2]
Строение полученного углеводорода ( 2 5-диметилгексина - З) доказано константами, анализом, а также окислением его в изомасляную кислоту, охарактеризованную температурой плавления ее анилида. [3]
Для доказательства строения полученного углеводорода было проведено его окисление. Процесс окисления длился 10 - 12 час. [4]
В процессе дегидратации двойная связь часто перемещается и строение полученного углеводорода не соответствует строению исходного спирта. [5]
В процессе дегидратации часто происходит перемещение двойной связи и строение полученного углеводорода не отвечает строению исходного спирта. [6]
Как видно из уравнения, выражающего превращение ( 1), кислоты, распадаясь на углеводород и углекислоту, могут стать источником образования углеводородов любого класса, так как радикал кислоты определяет характер и строение полученного углеводорода. В соответствии с тем, что известно о природе кислот сланцевой смолы, можно считать, что основную масс углеводородов, получающихся при разложении этих кислот, будут составлять парафины и олефины нормального строения, так как все карбоновые кислоты, которые известны и выделены из сланцевой смолы, принадлежат исключительно к жирным кислотам нормального строения. Это подтверждается и строением выделенных и изученных углеводородов сланцевой смолы. [7]
Синтез бициклононана был впервые осуществлен Меервейном [2], получившим этот углеводород сложным синтетическим путем. Строение полученного углеводорода достаточно надежно обосновано автором при исследовании различных химических превращений. [8]
Долгое время химиков-органиков занимал вопрос о существовании циклических систем с тройной связью в кольце, причем в экспериментальной и теоретической разработке этой интересной проблемы приняли участие из русских ученых В. В. Марковников, А. Е. Фаворский с учениками, а из зарубежных химиков Вильштеттер, Ружичка и др. Первое указание на возможность существования семичленного кольца с тройной связью сделал В. В. Марковников [207] в 1896 г. Отнимая 2 НВг от 1 2-дибромциклогеп-тана спиртовой щелочью, он получил углеводород С7Н1о, который принял за циклогептин. Других надежных доказательств строения полученного углеводорода не было приведено. [9]
Отсутствие молекулярной перегруппировки при пиролизе 12-кетохола-новой кислоты установлено на основании наблюдения, что дегидронорхолен может быть окислен до кетокислоты207, которая дает при восстановлении по Кижнеру2fis продукт, идентичный норхолановой кислоте. Кенэуэй и Кук 70, получившие незадолго до того синтетические канцерогенные вещества, считали возможным, что очень близкие по строению продукты могли бы получиться при циклизации боковой цепи желчных кислот. Независимо от них Кук и Хэзльуд268 получили метил-холантрен из дегидронорхолена и установили строение полученного углеводорода, превратив его окислением и последующим декарбокси-лированием в диметилбензантрахинон, идентифицированный синтезом. В схеме 18, приведенной ниже, разобран улучшенный синтез272, являющийся наилучшим препаративным методом получения этого углеводорода. [10]
Страницы: 1