Октаэдрическое строение
Cтраница 4
Молекула, в которой центральный атом образует пять связей и имеет одну неподеленную пару, может характеризоваться октаэдрическим строением, и в этом случае связи должны быть направлены к пяти вершинам квадратной пирамиды, а неподеленная пара должна занимать шестую вершину октаэдра. Было показано, что молекула BrF5 имеет именно такую конфигурацию. Отсюда следует, что вокруг атома брома неподеленная электронная пара занимает несколько большее пространство по сравнению с пространством, занимаемым поделенными парами. Аналогичным образом в аммиаке, воде и близких им по строению молекулах каждая неподеленная пара занимает больший телесный угол, чем поделенная пара. [46]
Комплексные ионы [ FefCNJg ] 4 - и [ Fe ( CN) 6 ] 3 - имеют октаэдрическое строение и Лг / Р - гибридное состояние орбиталей связи. [47]
Плоское строение для рассматриваемых элементов можно ожидать для их двухвалентного состояния, и как тетраэдрическое, так и октаэдрическое строение противоречит тому, чего следует ожидать по законам валентности, особенно для палладия и платины, обычно образующих ковалентные связи. Не следует, однако, удивляться, если правила валентности оказываются нарушенными в тех случаях, когда соблюдение их вызвало бы большие напряжения в органических радикалах; известны также и другие случаи подобного рода. [48]
 |
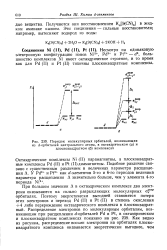
Энергетический порядок некоторых орбиталей рического ( а и плоскоквадратного ( 6 комплексов. [49] |
Несмотря на одинаковую электронную конфигурацию ионов Ni2, Pd2 и Pt2 - dB, большинство комплексов Ni имеет октаэдрическое строение, в то время как для Pd ( II) и Pt ( II) типичны плоскоквадратные комплексы. Октаэдричес-кие комплексы Ni ( II) парамагнитны, а плоскоквадратные комплексы Pd ( II) и Pt ( II) диамагнитны. [50]
 |
Порядок молекулярных орбиталей, возникающих. [51] |
Несмотря на одинаковую-электронную конфигурацию ионов Ni2 1, Pd2 и Pt2 - d8, большинство комплексов Ni имеет октаэдрическое строение, в то время как для Pd ( II) и Pt ( II) типичны плоскоквадратные комплексы. [52]
Несмотря на одинаковую электронную конфигурацию ионов Ni2, Pd2 и Pt2 - d8, большинство комплексов Ni имеет октаэдрическое строение, в то время как для Pd ( II) и Pt ( II) типичны плоско-квадратные комплексы. Октаэдр ические комплексы Ni ( II) парамагнитны, а плоскоквадратные комплексы Pd ( II) и Pt ( II) - диамагнитны. Подобное различие связано с существенным различием в величинах параметра расщепления А. [53]
 |
Перекрывание электронных облаков. [54] |
Наконец, молекулы АХ6 ( см. рис. 95, е), в том числе большинство комплексов, имеют октаэдрическое строение с прямыми углами между шестью связями ядра с лигандами. Такое же строение имеют гексафториды инертных газов. В этом случае неспаренный р-электрон атома фтора вступает в связь с одним из спаренных р-электронов внешней р6 - оболочки инертного газа. Таким образом, выявляется химическая активность ортогональной заполненной р - обо-лочки. [55]
Таким образом, было установлено, что закономерность трансвлияния в принципе осуществляется в комплексных соединениях, имеющих плоскостное или октаэдрическое строение. [56]
Страницы: 1 2 3 4