Влияние - добавка - соль
Cтраница 1
Влияние добавок солей на кислые и основные неэлектролиты различно. Основные неэлектролиты чувствительны к заряду аниона и всаливаются солями лития. [1]
Одновременно было исследовано влияние добавок солей таких металлов, как T1 ( I), Mn ( III), Се ( IV), Со ( III) и Cr ( VI), на ВТ реакции и распределение продуктов. [2]
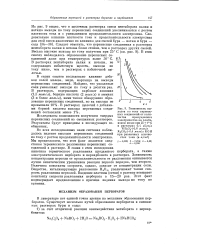 |
Зависимость выходов по току иерекис-ных соединений от количества пропущенного электричества на платиновом аноде при 25 1 С в растворах 0 4 моль / л. [3] |
В серии опытов исследовано влияние добавок солей железа, меди, марганца на выходы перекисных соединений. Найдено, что указанные соли уменьшают выходы по току в десятки раз. [4]
Бруйном 1 была сделана попытка определения С-потенциалов путем измерения влияния добавок солей на межфазные потенциалы. По теорий Штерна, двойной слой в воде состоит из плотно адсорбированной и диффузной частей, причем весь потенциал приходится на долю только диффузной части. В условиях, когда площадь поверхности и адсорбционная способность весьма велики, добавление соли к раствору должно изменять только ту часть межфазного потенциала, которая приходится на долю диффузной части двойного слоя. Тогда изменение межфазного потенциала равно изменению С-потенциала, и последнее может быть измерено. Подробные данные о результатах Бруйна пока отсутствуют. [5]
Большой прогресс в исследовании ионнопарного механизма был достигнут при изучении влияния добавок солей на скорости соль-волитических процессов. [6]
Из табл. 1 и рис. 1 следует, что действительно наблюдается полная аналогия во влиянии добавок солей на реакцию обмена и анионную со-полимеризацию. [7]
Предсказания теории качественно согласуются с зависимостями скоростей реакций от концентраций ПАВ для реакций первого, второго и третьего порядков, протекающих в различных экспериментальных условиях. Кроме того, удается объяснить влияние добавок солей на скорости реакций второго порядка. В ряде случаев уравнения используются для определения констант скоростей в мицеллярной фазе и констант ионного обмена. Полученные результаты согласуются с предположениями теории. В заключение на основании теорж предсказан ряд новых и подлежащих экспериментальной проверке результатов. [8]
Различные формы углерода, например графит и активные угли из разных источников, являются гетерогенными катализаторами разложения перекиси водорода, отличающимися рядом интересных особенностей. Активность углерода зависит от его происхождения [135]; кроме того, ее можно изменять специальной обработкой. Фоулер и Уолтон [136] исследовали влияние добавки солей или желатины на каталитическую активность активированного угля из сахара [ 136J; другие авторы изучали влияние температуры, размеров частиц, концентрации водородных ионов, излучения [137], концентрации перекиси водорода и химической природы поверхности угля. Однако эффективность катализа не является прямо пропорциональной этой адсорбции. Обработка поверхности, например нагреванием или пропусканием над ней азота [139], заметно изменяет активность. Активированный уголь из целлюлозы и рисового крахмала, высушенный при 100, обладает максимальной активностью; более слабым действием отличается уголь из декстрина, инулина и пшеничного крахмала; уголь из декстрозы, лактозы, мальтозы или картофельного крахмала едва ли обладает какой-либо активностью. [9]
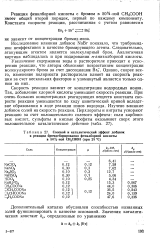 |
Солевой и каталитический эффект добавок. [10] |
Скорость реакции зависит от концентрации водородных ионов. Так, добавление хлорной кислоты уменьшает скорость реакции. При очень больших концентрациях реагирующих веществ константа скорости реакции уменьшается по ходу кинетической кривой вследствие образования в ходе реакции ионов водорода. Изучено влияние добавок солей на скорость реакции. [11]
Большая работа была проведена в области изучения термодинамических и структурных свойств смешанных растворов поверхностно-активных веществ ( ПАВ), их фазового поведения, в области моделирования мицел-лярных систем. Изучены диаграммы растворимости для водных смесей двух анионных ПАВ ( додецилсулъфаты натрия и калия, додецилдиэтокси-сульфат натрия), а также смесей анионного и цвитгерионного ПАВ. Установлена граница между мицеллярной и жидкокристаллической фазами, определены значения критических концентраций мицеллообразования ( ККМ) для индивидуальных веществ и смесей. Проведено исследование влияния добавок солей, органических соединений разных классов на смещение фазовых границ в растворах смешанных ПАВ. [12]
Первый член уравнения соответствует прямой, а второй - обратной реакции. Константы Kz и К увеличиваются с ПоВЬПпе-нием кислотности, причем К2 зависит от кислотности в ЭЩЧЙ-тельно большей степени, чем K f Определяемая зависимость скорости нитрования приводит к следующему; для 78 3 % - ной HaSO Ка 1 6 - 107ехр ( - 13230 / Д21), для 74 5 % - ной На804 Kz 7 7MQ7exp - 13790 / ДГ), для 81 1 % - ной H2S04 & t - 8 15 - 108ехр ( - 8940 / - R71), Изменение концентрации HN03 почти не влияет на величин 1 - К & При повыщенад КОЩрЮра-ции гуанидина константа К2 несколько падает. Это влияние как и влияние добавок неорганичерких солей, также понижающих эВДичдау Къ, повидимому, связано с изменением кислотности среды. [13]
Страницы: 1