Влияние - ион - металл
Cтраница 1
Влияние ионов металлов может и не носить ярко выраженный характер. [1]
Влияние иона металла, приводящее к необычным отношениям последовательных констант устойчивости, обычно сводится к электронным эффектам, таким, как переход от высокоспинового состояния к низкоспиновому или изменение гибридизации. Такое изменение состояния, высокоспинового на низкоспиновое, при взаимодействии железа ( II) с третьим лигандом вызывает аномально большое и благоприятное изменение энтальпии. Изменение гибридизации приводит не только к аномально высоким отношениям Kn iJKn, но и аномально низким отношениям этих констант устойчивости. Очень низкое значение Кз / К2 позволяет предположить, что при образовании HgX3 - из HgX2 происходит изменение sp - гибридизации на р3 - гибридизацию. [2]
Влияние ионов металлов на снижение растворимости кремнезема наиболее заметно в случае силикатных минералов. [3]
Эффект влияния ионов металлов, особенно меди, на реакцию ( 90) очень заметен, поэтому даже ничтожное содержание примесей вызывает резкое снижение выхода гидразина. Например, если применять обыкновенную воду, содержащую даже очень малые примеси ионов меди ( 1 ррт), и не вводить специальные добавки, то гидразин практически не образуется при использовании реактивов очень высокой чистоты. При работе с биди-стиллатом или тридистиллатом и тщательно очищенными сосудами, получается гидразин с приемлемыми выходами и без введения добавок. [4]
Примером влияния иона металла на реакционную способность путем стабилизации депротонированной формы лиганда может служить реакция хлористого 4-диметиламинофенилдиазония с хромотроповой кислотой. [5]
Под влиянием ионов металлов группы Б или переходных металлов СПЗ галогенидных или халькогенидных ионов могут смещаться в видимую область и, таким образом, сообщать окраску этим соединениям. Бромид серебра, например, имеет очень широкую полосу поглощения в видимой области, начинающуюся с 400 нм. В веществах, содержащих окрашенные ионы металлов, например, соединениях ионов переходных металлов с ионами галогенов, кислорода, суммарный спектр поглощения может состоять из спектра иона металла и СПЗ металлоида. [6]
Для определения влияния ионов металлов на неньютоновские свойства полимерных растворов были установлены зависимости вязкости полимерных растворов в водах различной минерализации от скорости сдвига. Оказалось, что с увеличением минерализации полимерного раствора уменьшаются его неньютоновские свойства, и при величинах минерализации, сопоставимых с обычно имеющимися на практике ( 50 - 100 г / л), полимерный раствор практически представляет собой ньютоновскую жидкость. [7]
В случае если влияние ионов металлов не может быть устранено, необходимо применить метод атомно-абсорбционной спектрометрии. [8]
В случае если влияние ионов металлов не может быть устранено, необходимо использовать метод атомно-абсорбционной спектроскопии. [9]
Исследования по выяснению влияния иона металла показали, что вместо никеля могут применяться другие металлы переменной валентности, наприме р двухвалентные кобальт и марганец и железо. Замена металла не вызывает существенного изменения клатратообразующих свойств комплекса; во всех случаях из ароматической фракции С8 избирательно связыватся п-ксилол. [10]
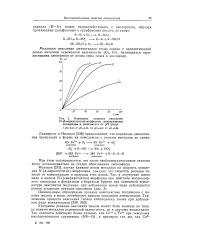 |
Изменение скорости окисления. [11] |
Францен [215], изучая влияние ионов металлов на скорость окисления Ы - ( р-меркаптоэтил) - морфолина, показал, что скорость реакции зависит от концентрации и природы этих ионов. [12]
Для более точной оценки влияния ионов металла на гидролиз эфира следует более детально разобраться в процессе взаимодействия лиганда и металла. В большинстве случаев эфир координируется с металлом, используя в качестве донорного атома только аминный азот. Карбонильная группа эфира, как и карбоксильная группа соответствующей аминокислоты, обладает слабыми нук-леофильными свойствами и не склонна к хелатообразованию. [13]
Одним из таких свойств является влияние иона металла на электронную структуру атакуемой карбонильной связи пептидного субстрата. Поскольку Zn ( II) - и Со ( П) - замещенные ферменты, вероятно, имеют сходное координационное окружение, для этих двух производных можно надеяться получить четкую корреляцию между искажениями электронной структуры карбонильной связи под действием иона металла и d - электронной конфигурацией металла. [14]
Поскольку взаимодействие металл-кислород существенно для гидролиза пептидов, представляется важным исследовать спектроскопически влияние ионов металлов, промотирующих гидролиз, на электронную структуру реакционноспособной карбонильной связи. [15]
Страницы: 1 2 3