Влияние - азотная кислота
Cтраница 1
Влияние азотной кислоты в нитрозе на упру - ость окислов азота. [1]
Влияние азотной кислоты на коэффициент распределения сложно. Увеличение концентрации азотной кислоты сначала увеличивает коэффициент распределения за счет увеличения концентрации экстрагируемого металла. Однако ТБФ сам образует экстрагируемый комплекс состава HNO3 - 3 ТБФ и, таким образом, между ионами металла и азотной кислотой происходит конкуренция за ТБФ, в результате чего извлечение металла уменьшается. Поэтому для увеличения концентрации нитрат-ионов добавляют - нитрат натрия, чтобы частично заменить азотную кислоту. [2]
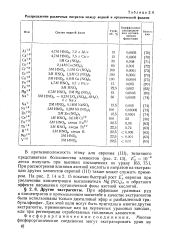 |
Распределение различных нитратов между водной и органической фазами. [3] |
При рассмотрении влияния азотной кислоты и нитратов на экстракцию других элементов европий ( III) также может служить примером. [4]
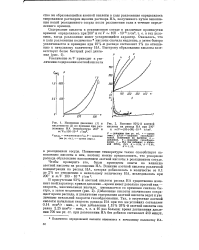 |
Изменение давления ( 1 и кислотности ( 2 по времени при разложении НА ( температура 200 и m / F 100 - 10 - 4 г / см3.| Влияние 93 % - и азотной. [5] |
Чтобы проверить это, были проведены опыты по влиянию азотной кислоты на разложение НА. [6]
Коноваловым было высказано предположение, что при нитровании под влиянием азотной кислоты окисляются не сами углеводороды, а лишь продукты нитрования. Из первичных нитросоединений при этом получаются альдегиды, выделить которые не удается, так как они окисляются до соответствующих кислот. [7]
Для решения проблемы материального оформления этого процесса было исследовано [178] влияние азотной кислоты на коррозионно-электрохимическое поведение сталей в серноазотных кислых смесях, содержащих 10 - 50 % H2SC4 и до 10 % НМОз. Показано, что при достижении определенной концентрации азотной кислоты потенциал сталей смещается в положительную сторону, происходит пассивация сталей, и скорость коррозии их резко уменьшается. [8]
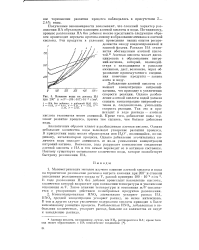 |
Влияние воды на распад НА при 200 и m / F ( 89 - 107 - 10 - 4 г / см3. [9] |
Полученные закономерности показывают, что сложный характер разложения НА обусловлен влиянием азотной кислоты и воды. По-видимому, процесс разложения НА без добавок можно представить следующим образом: происходит передача протона аниону и образование аммиака и азотной кислоты. Эти продукты в условиях проведения наших опытов распределяются между конденсированной и газовой фазами. Расплав НА становится обогащенным азотной кислотой. Азотная кислота может диссоциировать с образованием нитро-ний-катиона, который, взаимодействуя с находящимся в расплаве аммиаком, дает, возможно, через образование промежуточного соединения конечные продукты - закись азота и воду. [10]
Цветные, но прозрачные кольца на границе могут появиться от изменения мочевых или желчных пигментов под влиянием азотной кислоты. Моча, богатая солями мочевой кислоты, дает кольцо, которое получается не на границе азотной кислоты и мочи, а несколько выше. Моча, богатая мочевиной, может дать осадок, состоящий из плохо растворимой азотнокислой мочевины. Такое кольцо имеет кристаллический вид, кольцо же белка аморфно. Если при повторении реакции мочу предварительно развести водой, то кольца от мочевины не получится. [11]
Однако пинен может присоединять две молекулы воды. Под влиянием разведенной азотной кислоты пинен присоединяет сначала одну молекулу воды и превращается в терпинеол, а затем присоединяется вторая молекула воды, и получается терпин, то есть пинен превращается в производное ментана. Итак пинен, как и одноядерные терпены, отличается от ментана на 4 атома водорода, но только двух из них не хватает у соседних атомов углерода, вследствие чего устанавливается двойная связь; других двух атомов водорода не хватает, очевидно, у углеродных атомов, не стоящих рядом, вследствие чего возникает не двойная связь, а новое кольцо. [12]
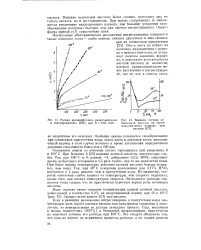 |
Распад предварительно разлагавшегося и эвакуированного НГЦ при б 0 03 - 0 04.| Влияние состава добавленной кислоты на время индукционного периода при распаде НГЦ. [13] |
При больших б [23] влияние азотной кислоты относительно слабее. Так, при 100 С и б, равной - 1, добавление 0 2 % HN03 сокращает время до быстрого ускорения в 1 5 раза слабее, чем то же количество воды. [14]
Так, ни одно уравнение не выражает всего, что в действительности происходит при действии металлов на азотную кислоту, так как образуется всегда несколько окислов азота вместе или последовательно - один за другим, по мере нагревания и изменения крепости кислоты. Образующийся окисел сам способен влиять на металлы и раскисляться, а под влиянием азотной кислоты он может изменять ее и сам изменяться. Написанные уравнения должно принимать как схематическое выражение главнейших видов реакции, как пре - Разложение закиси азота иеталли - дел, К которому стремится ДеЙСТВИтель-чсским натрием. [15]
Страницы: 1 2